El síndrome de fuga aérea (SFA) es una grave e infrecuente complicación no infecciosa del trasplante alogénico de médula ósea (TAMO) que afecta generalmente a pacientes con bronquiolitis constrictiva (BC) en el contexto de una enfermedad injerto contra huésped (EICH), y su pronóstico es muy pobre1–3. El diagnóstico del SFA suele ser radiológico y puede presentarse en forma de neumotórax, neumomediastino, enfisema intersticial y/o subcutáneo4,5. Presentamos el caso de un SFA tardío 22 años después de un TAMO en un paciente con antecedentes de leucemia aguda linfoblástica.
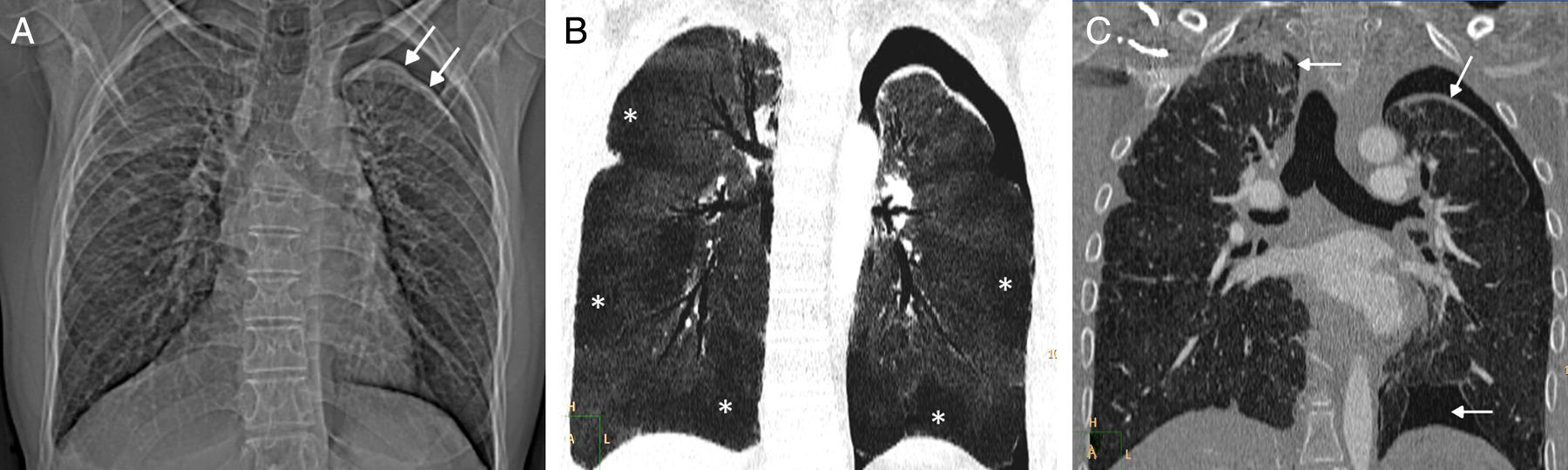
Se trata de un varón de 32 años que consultó en nuestro hospital por disnea de mínimos esfuerzos y dolor torácico. Entre sus antecedentes destacaba una leucemia linfoblástica aguda diagnosticada a los 6 años de edad y tratada con quimioterapia y radioterapia craneal profiláctica. Cuatro años después, a los 10 años de edad, sufrió una recaída testicular de su leucemia, sometiéndose a un TAMO tras un acondicionamiento con quimioterapia e irradiación corporal total. El paciente desarrolló varias complicaciones no infecciosas relacionadas con los tratamientos recibidos: hipogonadismo primario, cataratas bilaterales, déficit de hormona del crecimiento, síndrome de secreción inadecuada de hormona antidiurética, etc. Asimismo, a los 28 años de edad (18 años después del TAMO) al paciente se le diagnosticó una BC en el contexto de una EICH crónica grado I. Esta forma leve de EICH, que también presentaba manifestaciones cutáneas e intestinales se trató con dosis bajas de corticoides en un intento de minimizar el desarrollo de infecciones oportunistas, pero también porque las formas no severas de EICH tienen un efecto «injerto contra tumor» que reduce las posibilidades de recidiva tumoral. No obstante, las pruebas funcionales respiratorias del paciente fueron deteriorándose progresivamente a pesar de una escalada en la dosis de corticoides. Además el paciente presentó un primer episodio de neumotórax izquierdo (4 meses antes de ingresar en nuestro hospital) que fue tratado exitosamente con un tubo de drenaje en otro centro. En el momento del ingreso en nuestro centro el paciente presentaba una capacidad vital forzada de 1.230ml (27,2% del valor teórico de referencia) y un volumen espiratorio forzado de 1.060ml (27,7% del valor teórico de referencia). En una radiografía de tórax se identificó una pérdida de volumen de ambos pulmones y un nuevo neumotórax izquierdo (fig. 1A). En una TC de tórax se observaron signos de una BC con áreas de atrapamiento aéreo (fig. 1B) y un neumotórax bilateral (fig. 1C), emitiéndose el diagnóstico de SFA. A pesar de la colocación de un tubo de drenaje torácico izquierdo, el paciente falleció 5 semanas más tarde por una insuficiencia respiratoria.
A) Radiografía de tórax en la que se observa una pérdida de volumen de ambos pulmones y un neumotórax izquierdo (flechas). B) Reconstrucción coronal proyección de mínima intensidad (minIP) de la TC de tórax (ventana de parénquima pulmonar) que muestra áreas geográficas de baja atenuación en ambos pulmones (asteriscos) en relación con zonas de atrapamiento aéreo. C) Imagen coronal de la TC de tórax (ventana de parénquima pulmonar) en la que se identifica un neumotórax bilateral (flechas).
El SFA es una grave complicación no infecciosa del TAMO consistente en la presencia de gas extraalveolar en el tórax en forma de neumotórax, enfisema intersticial, neumomediastino y/o enfisema subcutáneo1. Se trata de una complicación muy poco frecuente, y la práctica totalidad de casos de SFA se asocian a cuadros avanzados de BC en el contexto de una EICH crónica2. No obstante, a diferencia de la presentación clínica generalmente larvada (disnea progresiva, taquipnea, tos) de la BC, el SFA puede manifestarse clínicamente de manera más aguda en forma de dolor torácico o disnea súbita. Además, el diagnóstico de SFA conlleva un pronóstico vital muy pobre a largo plazo, por lo que su detección radiológica tiene importantes implicaciones terapéuticas y pronósticas3. La mayor parte de los casos de SFA suele diagnosticarse desde pocos meses después del TAMO hasta 6-7 años después del mismo, y en general son las pruebas de imagen (especialmente la TC de tórax) las que confirman la sospecha clínica de SFA. A pesar de que la TC de tórax se ha convertido en una herramienta diagnóstica de gran utilidad en el diagnóstico y el seguimiento de las complicaciones relacionadas con el TAMO, existen muy pocas referencias bibliográficas que describan los hallazgos radiológicos del SFA4. Nuestro caso resulta interesante porque no hemos encontrado en la literatura científica un caso tan tardío de SFA tras un TAMO y porque solo se han descrito 3 casos previos de SFA con neumotórax bilateral5. Además, creemos que en pacientes sometidos a TAMO con diagnóstico (o sospecha clínica) de BC que presentan síntomas torácicos agudos (dolor torácico y/o disnea súbita) debe realizarse una TC de tórax para descartar las diferentes manifestaciones radiológicas del SFA.