El término hemoptisis hace referencia a la expectoración de sangre que se origina en el tracto respiratorio inferior1. Puede estar causada por enfermedades de las vías respiratorias, del parénquima pulmonar o de la vasculatura pulmonar, pero también puede ser idiopática1. La bronquitis crónica, las bronquiectasias y el carcinoma broncogénico son las causas más comunes en los países desarrollados1. Presentamos el caso de un paciente con hemoptisis, que fue atribuida al empleo de acenocumarol y que se controló con su sustitución por un anticoagulante oral de acción directa (ACOD).
Varón de 75 años, con antecedentes de exfumador (consumo acumulado: 30 paquetes-año), hipertensión arterial, diabetes mellitus, dislipidemia, ictus isquémico en territorio vertebrobasilar sin secuelas, angina de esfuerzo, fibrilación auricular permanente no valvular, anticoagulado con acenocumarol en rango terapéutico (CHA2DS2-VASc de 6 puntos, HAS-BLED de 1 punto), insuficiencia renal crónica secundaria a nefropatía diabética (creatinina 1,76mg/dl, filtrado glomerular 38ml/min/1,73m2), resección transuretral de vejiga por carcinoma urotelial de crecimiento papilar de bajo grado histológico, no invasivo (TaG1), que no precisó de tratamiento adyuvante y en remisión completa, polimialgia reumática, gota y varices intervenidas hace 5 años. En enero de 2018 acudió a urgencias por un cuadro de 2 meses de evolución de expectoración hemoptoica de escasa cuantía, por lo que fue ingresado para completar el estudio. La auscultación cardíaca mostraba tonos cardíacos arrítmicos, siendo el resto de la exploración física anodina. En la analítica destacaba una cifra de INR en rango de anticoagulación terapéutica y no se observaron alteraciones de carácter agudo en la radiografía de tórax. La tomografía computarizada (TC) torácica mostró un infiltrado en vidrio deslustrado en ambos lóbulos inferiores y en el lóbulo medio, que se acompañaba de engrosamiento liso de los septos interlobulillares. Ante estos hallazgos se plantearon, como diagnósticos posibles, un edema agudo de pulmón, sangre aspirada y una neumonía intersticial descamativa, recomendándose la realización de una nueva TC en un plazo aproximado de 3 meses. En la fibrobroncoscopia que se realizó se observó que ambos árboles bronquiales estaban permeables y la mucosa era de aspecto normal, no detectándose restos hemáticos a ningún nivel. Tanto la microbiología como la citología del aspirado bronquial fueron negativas. Ante estos hallazgos, el paciente fue dado de alta, tras reiniciar el tratamiento con acenocumarol, que se había suspendido durante el ingreso.
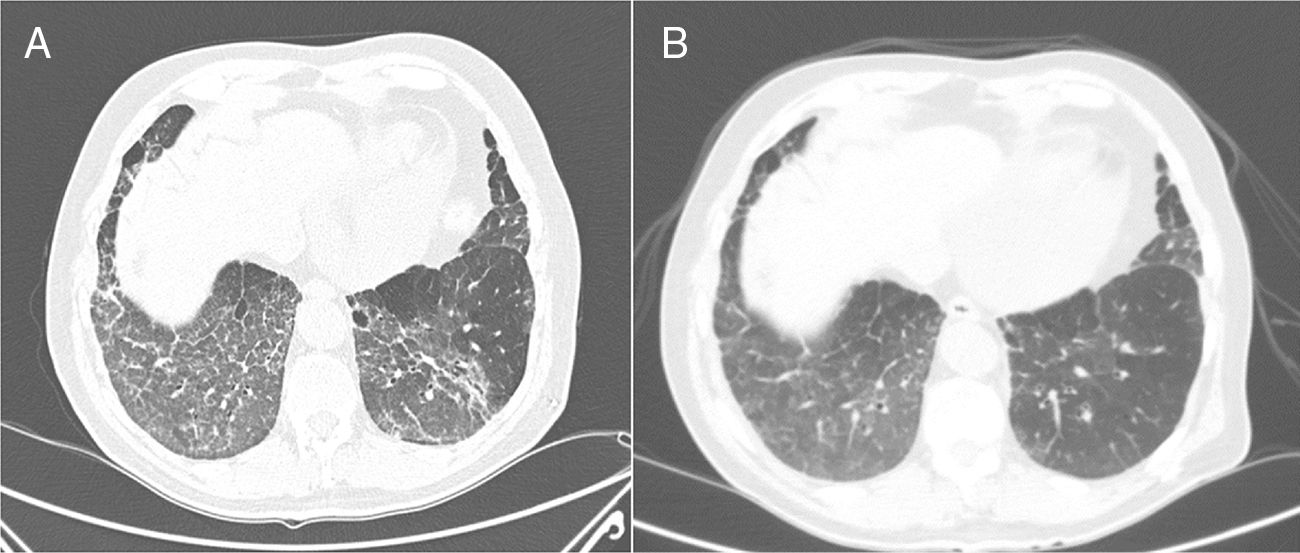
A los 3 meses el paciente refería que la hemoptisis persistía, aunque era de escasa cuantía. En la TC torácica de control se observó un infiltrado en vidrio deslustrado en ambas bases pulmonares y en el lóbulo medio, con engrosamiento lineal de septos interlobulillares asociado, que había aumentado de forma notable con respecto al estudio previo (fig. 1A). Ante estos hallazgos se repitió la fibrobroncoscopia y se realizó una biopsia transbronquial a nivel del lóbulo inferior derecho, que mostró cambios histológicos compatibles con neumonía organizada. Dado que se trataba de una hemoptisis de larga duración, sin lesiones endobronquiales que la justificasen y que podía estar relacionada con el tratamiento con acenocumarol, a pesar de que en los análisis de los últimos meses el INR estaba en rango terapéutico de anticoagulación (INR entre 2 y 3, con un tiempo en rango terapéutico acumulado del 65,5% y, desde la última medición, del 100%), se decidió suspender el tratamiento con acenocumarol e iniciar al día siguiente un ACOD, concretamente apixabán (su uso se ha asociado a menores tasas de sangrado en los ensayos clínicos). La dosis empleada fue de 5mg/12h, sin que se realizara ajuste de dosis, ya que el filtrado glomerular era mayor de 30ml/min/1,73m2.
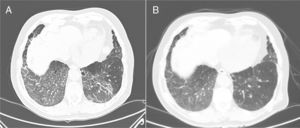
1A: Tomografía computarizada en la que se aprecia un infiltrado en vidrio deslustrado en ambas bases pulmonares y LM, con engrosamiento lineal asociado de septos interlobulillares. 1B: Tomografía axial computarizada de control, realizada a los 3 meses del cambio de tratamiento de acenocumarol por apixabán, con un tenue infiltrado en vidrio deslustrado parcheado en bases, con mejoría significativa con respecto a la previa.
En las revisiones posteriores el paciente refería disminución progresiva de la expectoración hemoptoica hasta su desaparición. En la TC torácica realizada a los 3 meses del estudio previo se observó un tenue infiltrado en vidrio deslustrado, parcheado en las bases, con mejoría significativa respecto al estudio previo (fig. 1B). En las pruebas de función respiratoria se obtuvieron los siguientes valores: FEV1 2.200ml (97,5%), FVC 3.400ml (114%), FEV1/FVC 64,67%, DLCO 81,5% y KCO 105,1%. Dada la mejoría se decidió continuar con apixabán, no volviendo a presentar el paciente incidencia alguna durante el seguimiento posterior.
Un 0,5% de la población usa anticoagulantes orales, siendo los más empleados los antagonistas de la vitamina K (AVK)2. La complicación más importante relacionada con su uso es la hemorragia, que se asocia a un aumento de la mortalidad2–4. La terapia anticoagulante también es un factor de riesgo para el desarrollo de hemorragias de origen respiratorio, con o sin enfermedades crónicas respiratorias previas, aumentando la posibilidad de sangrado en caso de padecerlas5. Entre los factores que aumentan el riesgo hemorrágico se encuentran los siguientes: edad avanzada, sexo femenino, antecedente de hemorragias previas, hipertensión arterial no controlada, insuficiencia renal, hepatopatía, anemia, empleo concomitante de antiagregantes y uso regular de agentes antiinflamatorios2,4. El excesivo efecto antitrombótico (INR>3 o INR entre 2 y 3 más antiagregación) es un factor reconocido que favorece el sangrado. No obstante, un 20% de los sangrados mayores en una serie italiana ocurrieron con un valor de INR<2, por lo que es importante prestar atención al resto de los factores que pueden incrementar el riesgo de sangrado4.
Desde el año 2008 se han ido introduciendo los ACOD, incluyendo los inhibidores orales del factor Xa (rivaroxabán, edoxabán y apixabán) y el inhibidor oral de la trombina (dabigatrán), primero para la prevención primaria de enfermedad tromboembólica venosa en adultos sometidos a cirugía programada de reemplazo de cadera o rodilla, después para reducir el riesgo de ACV y embolia sistémica en pacientes con fibrilación auricular no valvular, y posteriormente en la profilaxis secundaria de la enfermedad tromboembólica venosa, encontrándose también indicados en otras situaciones, como la prevención secundaria en pacientes adultos que han sufrido un síndrome coronario agudo con elevación de biomarcadores en el caso de rivaroxabán2,3,6. Los ACOD aportan ventajas con respecto a los AVK, como el rápido comienzo de acción, la no necesidad de monitorización rutinaria, una relación dosis-respuesta más predecible, una vida media plasmática más corta, un riesgo bajo de efectos adversos, pocas interacciones con fármacos y alimentos, una eficacia mejorada, y disponibilidad de antídoto específico (idarucizumab) en el caso de dabigatrán, encontrándose también otros en vías de aprobación (andexanet) como antídoto general de los inhibidores del factor Xa2,4,7. Pero los ACOD, como cualquier tratamiento anticoagulante, siempre conllevan un riesgo de sangrado por factores asociados al paciente, que puede verse incrementado en algunas situaciones como la sobredosis, las enfermedades o tratamientos concomitantes que aumentan la exposición al fármaco, las alteraciones de la hemostasia o la realización urgente de un procedimiento invasivo o quirúrgico3,4. En los ensayos clínicos con ACOD, las tasas de hemorragia fueron generalmente bajas y comparables a las producidas por las heparinas de bajo peso molecular o la warfarina en el caso de dabigatrán y rivaroxabán, o significativamente menores para el apixabán (en el ensayo ARISTOTLE, la tasa de hemorragia mayor fue del 2,13% por año en el grupo de apixabán en comparación con el 3,09% por año en el grupo de warfarina, RR: 0,69; IC 95%: 0,60-0,80, p<0,001)3,8. En este sentido, las guías actuales de cardiología recomiendan el uso preferente de los ACOD frente a los AVK en los pacientes con fibrilación auricular no valvular9.
En conclusión, la anticoagulación es un factor predisponente para el desarrollo de hemorragia, incluyendo el origen pulmonar. La sobredosificación, en el caso de los AVK, es un factor de riesgo importante de esta complicación, pero también hay que tener en cuenta otros factores que pueden incrementar el riesgo de sangrado. Los ACOD presentan ventajas con respecto a los AVK, aunque como cualquier tratamiento anticoagulante siempre conllevan un riesgo de sangrado por factores asociados al paciente.