Puntos clave:
- •
La agudización se define como un episodio agudo de inestabilidad clínica caracterizado por un empeoramiento mantenido de síntomas respiratorios.
- •
Es necesario distinguir una nueva agudización de un fracaso terapéutico previo o de una recaída.
- •
El diagnóstico de una agudización de la EPOC consta de 3 pasos esenciales: a) diagnóstico diferencial; b) establecer la gravedad, y c) identificar su etiología.
- •
En la agudización de la EPOC de cualquier intensidad, la principal intervención es optimizar la broncodilatación, aumentando la dosis y/o la frecuencia de los broncodilatadores de acción corta.
- •
Los antibióticos están especialmente indicados en presencia de esputo purulento.
- •
Se deberá emplear una pauta corta de corticoides sistémicos en las agudizaciones moderadas, graves o muy graves.
- •
La administración de oxígeno, cuando esté indicada, debe realizarse siempre de forma controlada.
- •
La ventilación mecánica no invasiva (VMNI) se debe valorar en todo paciente que curse con acidosis respiratoria (pH < 7,35).
La agudización o exacerbación se define como un episodio agudo de inestabilidad clínica que acontece en el curso natural de la enfermedad y se caracteriza por un empeoramiento mantenido de los síntomas respiratorios. Desde el punto de vista fisiopatológico, las agudizaciones son eventos complejos habitualmente relacionados con un incremento de la inflamación local y sistémica, aumento de la producción de moco y un marcado atrapamiento aéreo. Estos cambios contribuyen a la aparición de síntomas, como el empeoramiento de la disnea, la tos, el incremento del volumen y/o los cambios en el color del esputo.
Habitualmente estos cambios sintomáticos se acompañan de modificaciones en la medicación, y por eso en muchos ensayos clínicos y estudios epidemiológicos se valora la utilización de fármacos (antibióticos y/o corticoides sistémicos) o el uso de recursos sanitarios (visitas a urgencias, hospitalizaciones, etc.) como marcadores indirectos de agudización. Sin embargo, utilizando registros diarios de síntomas, se ha observado que más de la mitad de las agudizaciones no se comunican al médico (agudizaciones no documentadas)1,2.
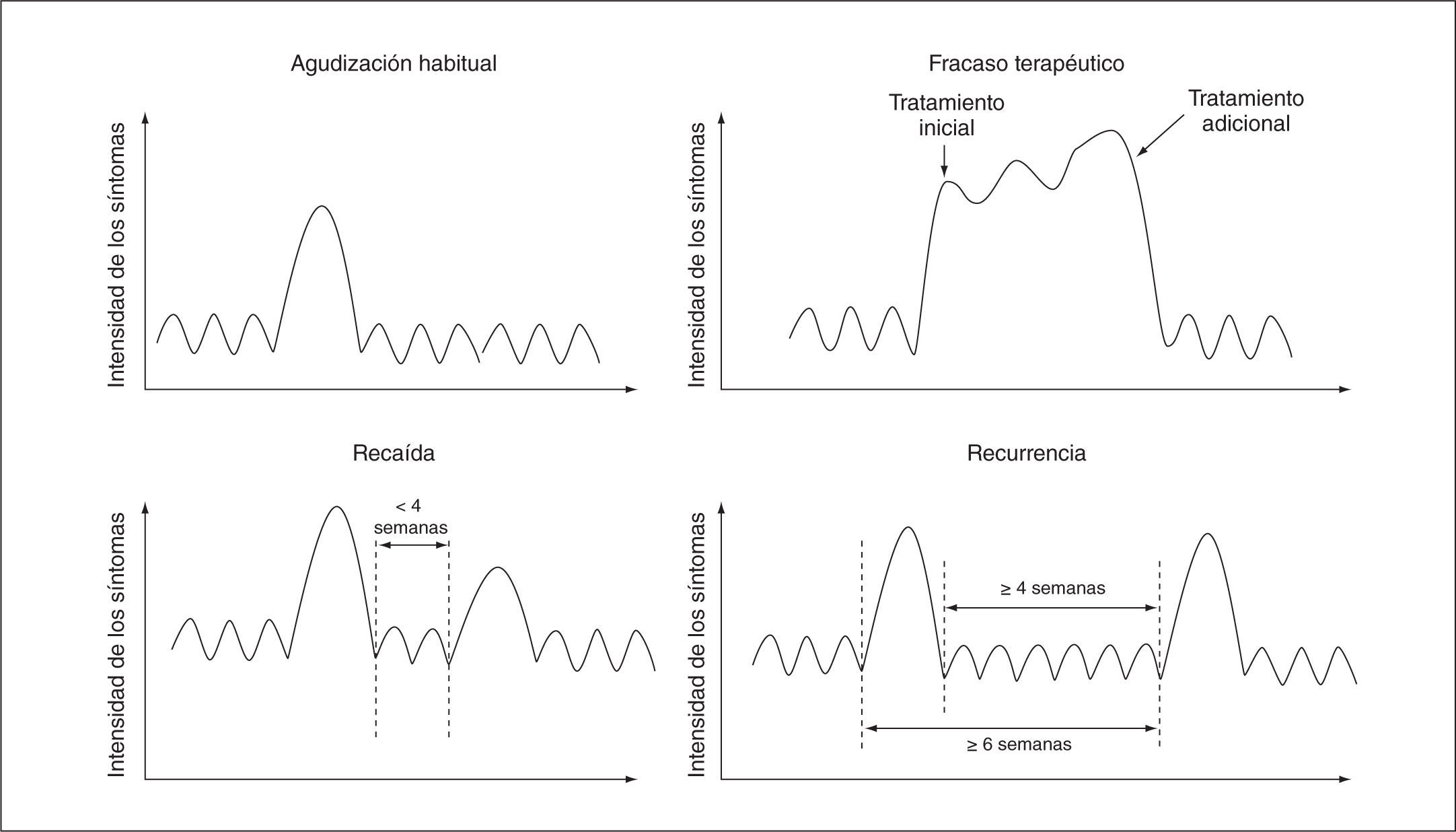
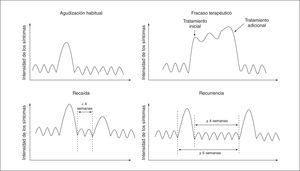
En promedio, los pacientes con EPOC experimentan 1-4 exacerbaciones/año3. Sin embargo, la distribución es muy variable. Mientras algunas personas no presentan estos episodios, otras lo hacen de forma repetida (fenotipo agudizador)4. Muchos de estos episodios se observan agrupados en racimos5, lo que plantea la duda de si realmente son nuevas exacerbaciones o son resoluciones incompletas del episodio precedente. Para distinguir estas situaciones, GesEPOC establece las siguientes definiciones (fig. 1):
- •
Fracaso terapéutico: se define como un empeoramiento de síntomas que sucede durante la propia agudización y que requiere un
- •
tratamiento adicional6. La recuperación media después de experimentar una agudización es de aproximadamente 2 semanas. No obstante, algunos pacientes no se recuperan de forma completa hasta las 4-6 semanas7,8.
- •
Recaída: cuando se produce un nuevo empeoramiento de síntomas entre la finalización del tratamiento de la agudización y las 4 semanas posteriores.
- •
Recurrencia: se produce cuando los síntomas reaparecen en un plazo inferior a un año desde la agudización precedente, después de un período de relativo buen estado de salud. Para ello se establece que deben haber transcurrido al menos 4 semanas después de completar el tratamiento de la agudización previa o bien 6 semanas desde que se iniciaron los síntomas6. Las recurrencias son nuevas agudizaciones que se producen en un mismo año. Se considerarán precoces si aparecen entre 4 y 8 semanas tras el episodio anterior, y tardías si aparecen después de este intervalo de tiempo.
La intensidad, la duración y la frecuencia de las agudizaciones varían enormemente de unos pacientes a otros e incluso en el mismo paciente, por lo que resulta difícil precisar sus consecuencias. Sin embargo, distintos estudios han demostrado que las agudizaciones producen un deterioro de la calidad de vida relacionada con la salud (CVRS), generan elevados costes, afectan a la progresión multidimensional de la enfermedad y aumentan el riesgo de muerte1,2,9–11.
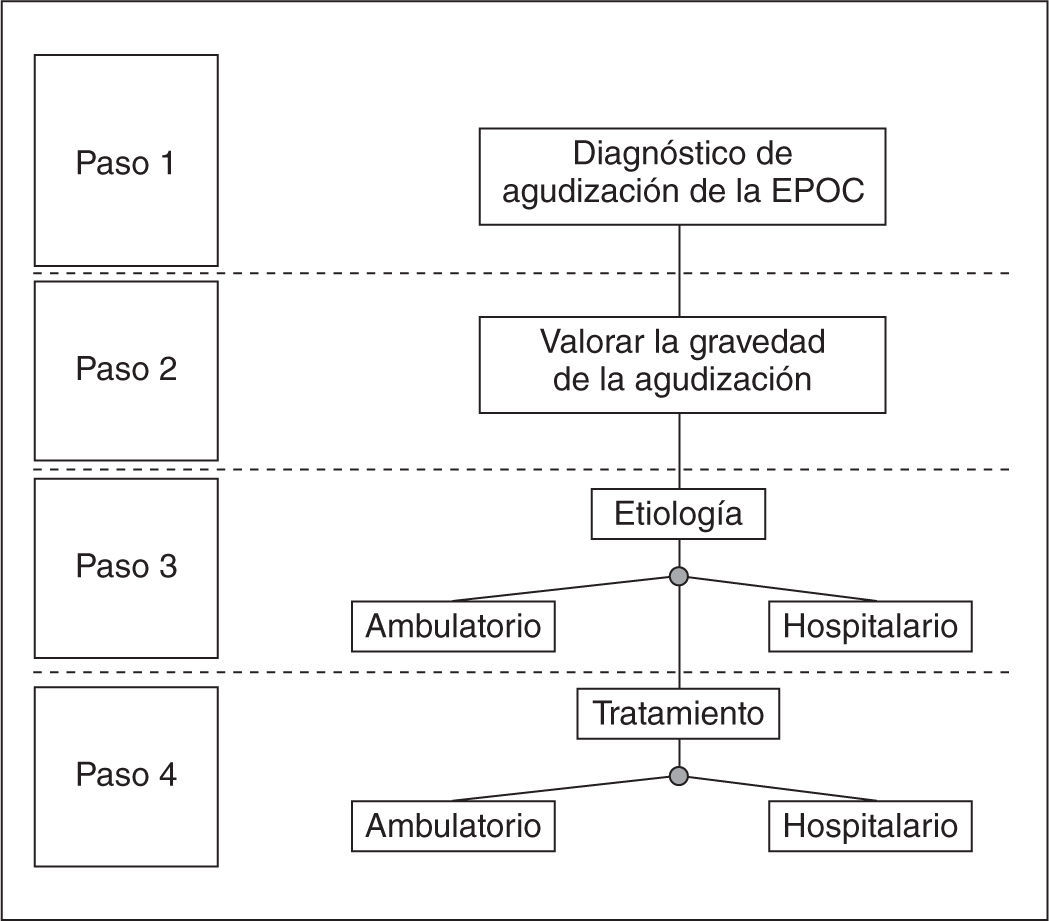
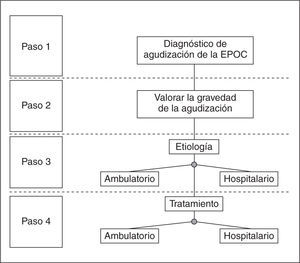
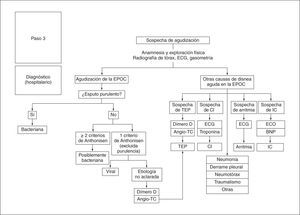
DiagnósticoEn la figura 2 se establecen los 3 pasos diagnósticos que hay que seguir para caracterizar adecuadamente una agudización. En primer lugar, se deberá confirmar que se trata de una agudización de la EPOC, descartando otros procesos que cursan con síntomas similares; en segundo lugar, se valorará la gravedad de la agudización, y finalmente se intentará establecer su causa. Para este último punto, las pruebas diagnósticas que hay que realizar pueden diferir según se trate de una agudización ambulatoria u hospitalaria.
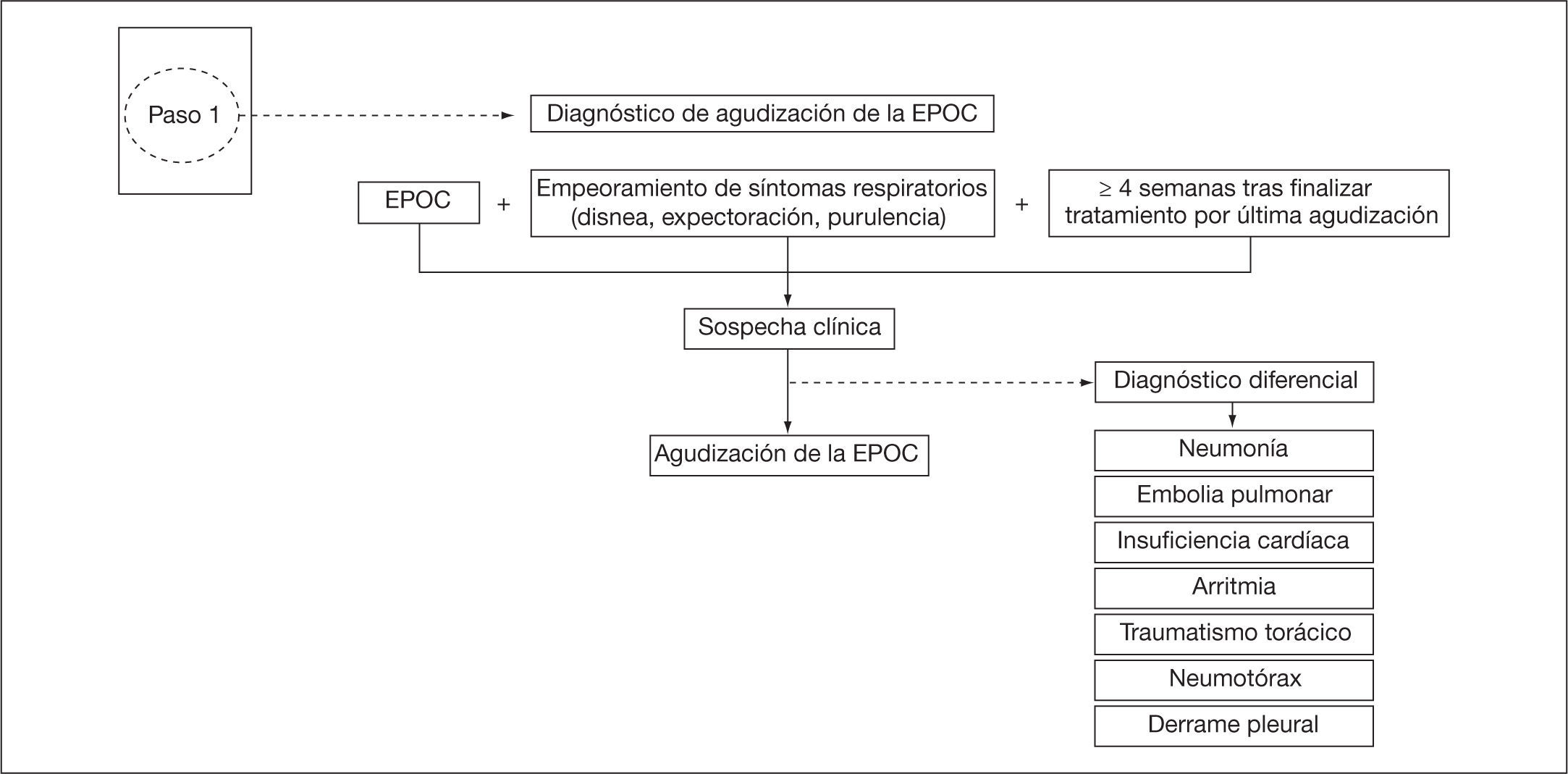
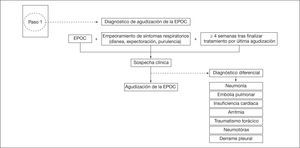
Paso 1: diagnóstico de agudización de EPOCLa sospecha clínica de una agudización de EPOC se establecerá cuando se den los siguientes 3 criterios:
- 1.
Diagnóstico previo de EPOC. En los casos donde no esté previamente diagnosticada la EPOC con certeza y no se disponga de espirometría, no podrá establecerse el diagnóstico de EPOC y, por tanto, tampoco el de agudización de EPOC. En estos casos se recomienda utilizar el término “posible agudización de EPOC”. Una vez estabilizado el paciente, se deberá realizar una espirometría para confirmar el diagnóstico.
- 2.
Empeoramiento mantenido de síntomas respiratorios, especialmente aumento de la disnea respecto a la situación basal, aumento del volumen del esputo y/o cambios en su coloración. Para documentar que existe empeoramiento de síntomas se deberá conocer y describir cuál es la situación basal del paciente. Para valorar el grado de disnea se recomienda utilizar la escala modificada de la Medical Research Council (mMRC).
- 3.
No haber recibido tratamiento para otra agudización en las últimas 4 semanas. Si el paciente ha recibido tratamiento en las últimas 4 semanas por otra agudización no se puede etiquetar de nueva agudización, sino de recaída o fracaso terapéutico de la previa.
Se confirmará el diagnóstico de agudización de EPOC en los casos en que, además de cumplir los 3 criterios previos, se hayan descartado otras causas secundarias de disnea (fig. 3 y tabla 1).
Diagnóstico diferencial ante un deterioro de síntomas en pacientes con EPOC
| Causas respiratorias: |
| Neumonía |
| Neumotórax |
| Embolia pulmonar |
| Derrame pleural |
| Traumatismo torácico |
| Causas cardíacas: |
| Insuficiencia cardíaca |
| Arritmias cardíacas |
| Cardiopatía isquémica aguda |
| Otras causas: |
| Obstrucción de vía aérea superior |
En la tabla 1 se muestran las principales enfermedades que cabe considerar en el diagnóstico diferencial de la agudización de la EPOC. Todas estas otras enfermedades también producen aumento de síntomas respiratorios en pacientes con EPOC, especialmente disnea. Sin embargo, la fisiopatología es distinta y el tratamiento, también, por lo que no se deben contemplar como causa de agudización, sino como diagnósticos alternativos.
En algunas ocasiones, la agudización de la EPOC se asocia a algunas de las enfermedades que figuran como diagnóstico diferencial y en tales casos resulta muy difícil discriminar cuál es la causa y cuál, la consecuencia. En estos casos se recomienda utilizar el término “agudización de EPOC asociada a...”. Por ejemplo, se ha descrito que hasta un 30% de las agudizaciones graves se asocian a insuficiencia cardíaca12, o que un 15-20% se asocia a daño miocárdico con elevación de troponinas13.
Fenotipos de agudizaciónLa agudización de la EPOC, al igual que sucede con la propia enfermedad de base, es heterogénea y compleja. Algunos estudios apuntan a la existencia de diferentes grupos o fenotipos clínicos de agudización14, con diferentes mecanismos biológicos (endotipos) subyacentes. De confirmarse estos postulados, el tratamiento de la exacerbación podría personalizarse. Se ha sugerido que las exacerbaciones que cursan con incremento de eosinófilos en esputo o sangre periférica pueden responder mejor a los corticoides sistémicos15. Sin embargo, se necesitan más evidencias para poder establecer recomendaciones específicas.
Paso 2: Valorar la gravedad de la agudizaciónUna vez establecido el diagnóstico de agudización de la EPOC es muy importante describir la gravedad del episodio. En la tabla 2 se exponen los criterios de gravedad propuestos por GesEPOC. Los criterios de agudización grave o muy grave identifican riesgo de muerte, mientras que los criterios que se utilizan para identificar la agudización moderada están relacionados con el riesgo de fracaso terapéutico.
Criterios para establecer la gravedad de la agudización de la EPOC
| Agudización muy grave (o amenaza vital) | Se debe cumplir al menos 1 de los siguientes criterios: |
| – Parada respiratoria | |
| – Disminución del nivel de consciencia | |
| – Inestabilidad hemodinámica | |
| – Acidosis respiratoria grave (pH < 7,30) | |
| Agudización grave | Se debe cumplir al menos 1 de los siguientes criterios, y ninguno de los criterios de amenaza vital: |
| – Disnea 3-4 de la escala mMRC | |
| – Cianosis de nueva aparición | |
| – Utilización de musculatura accesoria | |
| – Edemas periféricos de nueva aparición | |
| – SpO2 < 90% o PaO2 < 60 mmHg | |
| – PaCO2> 45 mmHg (paciente sin hipercapnia previa) | |
| – Acidosis respiratoria moderada (pH: 7,30-7,35) | |
| – Comorbilidad significativa grave* | |
| – Complicaciones (arritmias graves, insuficiencia cardíaca, etc.) | |
| Agudización moderada | Se debe cumplir al menos 1 de los siguientes criterios, y ninguno de los anteriores: |
| FEV1 basal < 50% | |
| – Comorbilidad cardíaca no grave | |
| – Historia de 2 o más agudizaciones en el último año | |
| Agudización leve | No se debe cumplir ningún criterio previo |
FEV1 volumen espiratorio forzado en el primer segundo; mMRC: escala de disnea modificada del Medical Research Council; PaCO2; presión arterial de dióxido de carbono; PaO2; presión arterial de oxígeno; SpO2: saturación parcial de oxígeno.
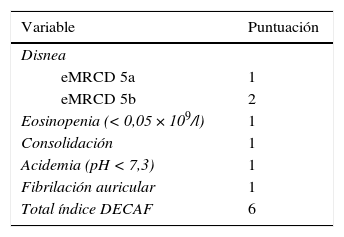
Disponer de escalas predictivas de riesgo puede ser de gran interés de cara a estratificar a los pacientes y diseñar actuaciones asistenciales de diferente intensidad y/o complejidad. Steer et al16 han desarrollado el índice DECAF (disnea basal, eosinopenia, consolidación, acidemia y fibrilación auricular) a partir de los 5 predictores de mortalidad con más peso específico (tabla 3). La disnea basal durante la fase estable de la enfermedad se valoró mediante la escala de la Medical Research Council extendida (eMRCD). En la escala, el grado 5 de disnea, que equivale al grado 4 de la escala mMRC recomendada por GesEPOC, se ha subdividido en 5a (para pacientes que son capaces de lavarse o vestirse de forma independiente) y 5b (para los que requieren asistencia para ambas tareas). Este índice mostró una excelente discriminación para mortalidad con un estadístico C de 0,86 (intervalo de confianza [IC] del 95%, 0,82-0,89) y fue más preciso que otros predictores clínicos de mortalidad16,17.
Índice DECAF para pacientes hospitalizados por agudización de EPOC
| Variable | Puntuación |
|---|---|
| Disnea | |
| eMRCD 5a | 1 |
| eMRCD 5b | 2 |
| Eosinopenia (< 0,05 × 109/l) | 1 |
| Consolidación | 1 |
| Acidemia (pH < 7,3) | 1 |
| Fibrilación auricular | 1 |
| Total índice DECAF | 6 |
DECAF: disnea, eosinopenia, consolidación, acidemia y fibrilación auricular; eMRCD: escala de la Medical Research Council extendida. Tomada con permiso de Steer et al16.
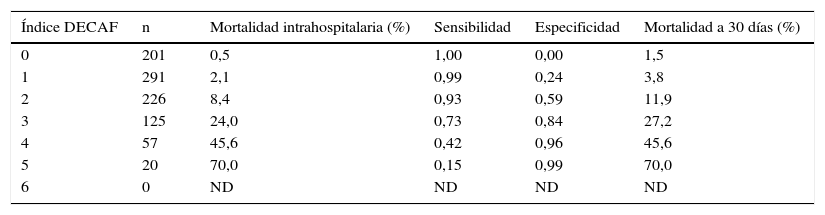
La tabla 4 muestra la mortalidad intrahospitalaria y a los 30 días tras hospitalización tras aplicar DECAF. Recientemente, se ha validado el índice DECAF (validación interna y externa) que ha demostrado ser un robusto predictor de mortalidad18. Uno de los aspectos controvertidos de DECAF es que incluye la presencia de consolidación entre los ítems que hay que valorar. Actualmente, la presencia de neumonía en un paciente con EPOC excluiría el diagnóstico de agudización de EPOC. Sin embargo, de forma pragmática, el índice DECAF resultar útil tanto para la agudización de EPOC como para la neumonía en paciente con EPOC.
Índice DECAF y mortalidad intrahospitalaria*
| Índice DECAF | n | Mortalidad intrahospitalaria (%) | Sensibilidad | Especificidad | Mortalidad a 30 días (%) |
|---|---|---|---|---|---|
| 0 | 201 | 0,5 | 1,00 | 0,00 | 1,5 |
| 1 | 291 | 2,1 | 0,99 | 0,24 | 3,8 |
| 2 | 226 | 8,4 | 0,93 | 0,59 | 11,9 |
| 3 | 125 | 24,0 | 0,73 | 0,84 | 27,2 |
| 4 | 57 | 45,6 | 0,42 | 0,96 | 45,6 |
| 5 | 20 | 70,0 | 0,15 | 0,99 | 70,0 |
| 6 | 0 | ND | ND | ND | ND |
DECAF: disnea, eosinopenia, consolidación, acidemia y fibrilación auricular; ND: no disponible.
Se consideró bajo riesgo: índice DECAF 0-1; riesgo intermedio: índice DECAF 2; riesgo alto: índice DECAF ≥ 3 puntos. Tomada con permiso de Steer et al16.
En la tabla 5 se recogen las causas más frecuentes de agudización de la EPOC19,20. Identificarlas es de gran importancia para un adecuado tratamiento. Sin embargo, en aproximadamente un tercio de los casos la etiología no se llega a conocer. Entre el 50 y el 70% de las ocasiones, la causa de la exacerbación es la infección del árbol traqueobronquial. La contaminación ambiental puede ser la causante del 5-10% de las exacerbaciones.
Causas de agudización de la EPOC
| Virus | Rinovirus (resfriado común) |
| Parainfluenza | |
| Influenza | |
| Coronavirus | |
| Adenovirus | |
| Virus respiratorio sincitial | |
| Bacterias | Haemophilus influenzae |
| Streptococcus pneumoniae | |
| Moraxella catarrhalis | |
| Pseudomonas aeruginosa | |
| Organismos atípicos | Chlamydophila pneumoniae |
| Mycoplasma pneumoniae | |
| Polución ambiental | Ozono |
| Partículas ≤ 10μm de diámetro | |
| Dióxido de sulfuro | |
| Dióxido de nitrógeno |
Las infecciones virales representan cerca del 30% de todas las exacerbaciones de causa infecciosa, aunque algunos estudios recientes que emplean técnicas diagnósticas más precisas elevan hasta el 50% el número de exacerbaciones infecciosas causadas por virus. Las bacterias identificadas con mayor frecuencia son Haemophilus influenzae, Streptococcus pneumoniae y Moraxella catarrhalis; aunque en agudizaciones graves, las enterobacterias y Pseudomonas aeruginosa pueden ser frecuentes21. La presencia de coinfección por bacterias y virus se ha descrito hasta en un 25% de los pacientes hospitalizados, lo que sugiere una cierta susceptibilidad a la infección bacteriana tras el proceso viral20.
Reconocer la etiología de la agudización no resulta sencillo. El análisis del esputo (tinción de Gram y cultivo) estará especialmente indicado en los pacientes con agudizaciones graves o muy graves que presenten frecuentes agudizaciones, necesidad de ventilación asistida o ante un fracaso del tratamiento antibiótico. Sin embargo, en la mayoría de los casos la aproximación diagnóstica será clínica. Anthonisen et al22 demostraron que la administración de antibióticos en la EPOC era más eficaz que el placebo en las agudizaciones que cumplían al menos dos de los siguientes tres criterios: aumento de disnea, purulencia en el esputo o aumento del volumen del esputo. Sin embargo, de los tres criterios recomendados, el que mejor predice la infección bacteriana es el cambio en la coloración del esputo (purulencia)23. Por el contrario, el esputo mucoso pocas veces se asocia a infección bacteriana24.
Existe una gran actividad de investigación sobre biomarcadores de infección bacteriana en las agudizaciones. En un metaanálisis reciente se sugiere que la procalcitonina podría ser de utilidad para disminuir la prescripción de antibióticos, sin que afecte a la tasa de fracasos terapéuticos, la duración de hospitalización, la recurrencia o la mortalidad25. Sin embargo, debido a limitaciones metodológicas, la evidencia todavía es baja o moderada, por lo que de momento no se puede establecer una recomendación general de uso de este biomarcador para establecer la etiología de una agudización.
Para tratar de identificar la causa de la agudización y establecer adecuadamente el diagnóstico diferencial, se propone una aproximación diferente según el nivel asistencial donde se atienda la descompensación.
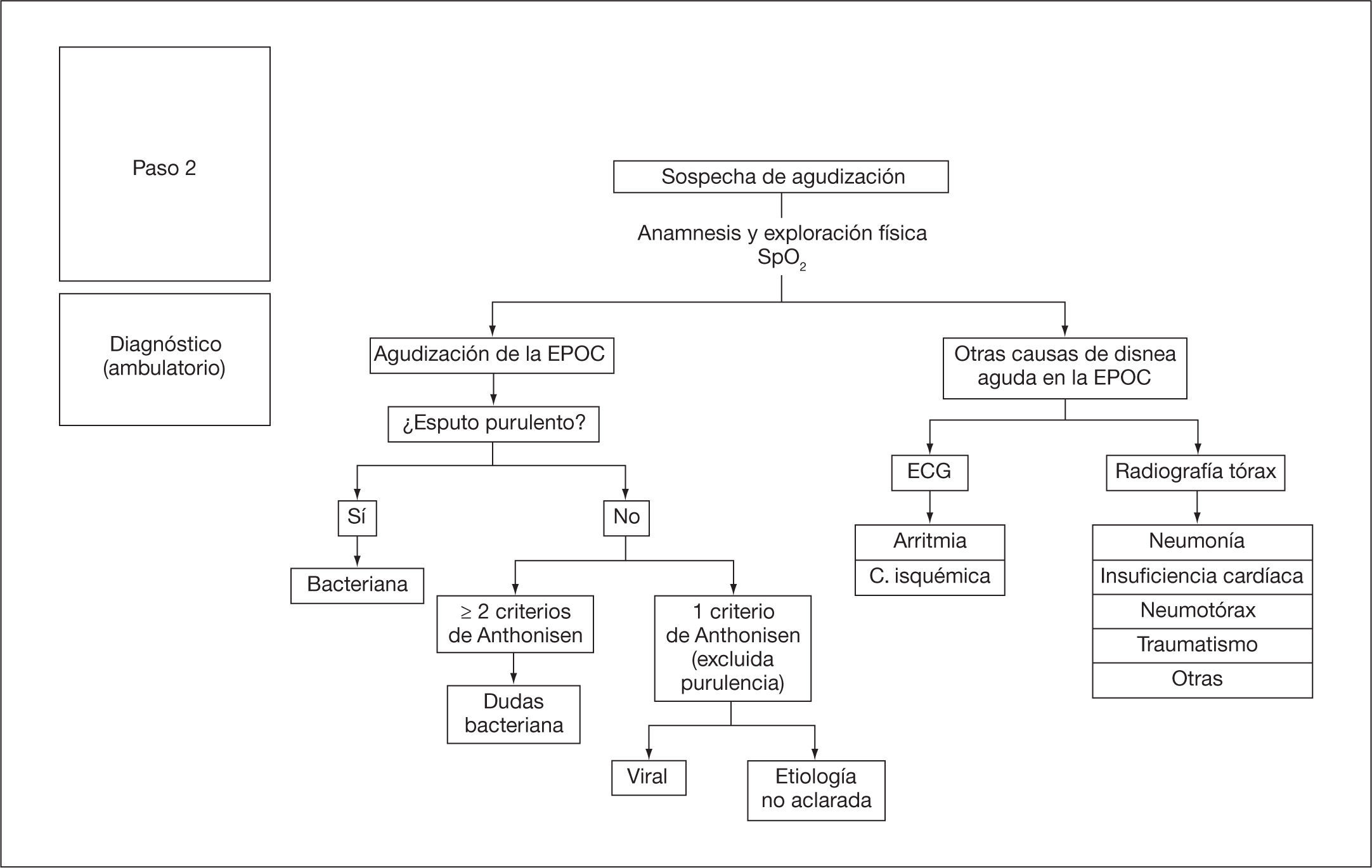
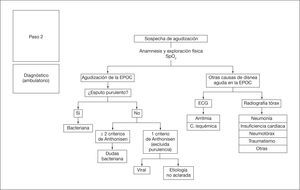
Aproximación diagnóstica ambulatoriaLa figura 4 señala el proceso diagnóstico que se debe realizar en el ámbito ambulatorio. A todos los pacientes se les deberá realizar una anamnesis y exploración física, de acuerdo con los criterios que se establecen a continuación. También es recomendable que se evalúe la saturación arterial de oxígeno (SaO2).
Historia clínica. La historia clínica de toda agudización deberá contener como mínimo la siguiente información:
- 1.
Sintomatología de la agudización:
- •
Disnea.
- •
Color del esputo.
- •
Volumen del esputo.
- •
- 1.
Historial de agudizaciones previas:
- •
La presencia de 2 o más agudizaciones moderadas o graves previas en el último año es un factor de riesgo de fracaso terapéutico (fenotipo agudizador). Por este motivo, su sola aparición ya indica agudización moderada y un tratamiento diferencial.
- •
- 1.
Comorbilidad.
- 2.
Gravedad basal de la EPOC.
- 3.
Tratamiento previo.
Exploración física. En la exploración física, se deberá registrar:
- 1.
Nivel de consciencia.
- 2.
Cianosis.
- 3.
Utilización de la musculatura accesoria.
- 4.
Edemas.
- 5.
Presión arterial.
- 6.
Frecuencia respiratoria y cardíaca.
- 7.
Temperatura corporal.
Pulsioximetría. Se aconseja el uso de la pulsioximetría, que evalúa de forma no invasiva la SpO2. Sin embargo, esta no mide la PaCO2 (presión arterial de dióxido de carbono) o el pH. Por tanto, no sustituye a la gasometría en la valoración del intercambio de gases, especialmente en situaciones críticas o donde haya sospecha de hipoventilación (hipercapnia).
El primer paso para reconocer la agudización de la EPOC es descartar la presencia de otras causas de empeoramiento sintomático (v. diagnóstico diferencial, tabla 1).
- •
Radiografía de tórax: no se recomienda realizar la radiografía de tórax de rutina en medio ambulatorio. Sin embargo, sí será pertinente en el caso de mala evolución clínica o sospecha de complicación (neumonía, insuficiencia cardíaca, etc.).
- •
Electrocardiograma (ECG): permite descartar arritmias o valorar signos de cardiopatía isquémica, por lo que está indicado en caso de sospecha.
Una vez confirmada la agudización de la EPOC, se deberá valorar el color del esputo. En caso de un cambio de color, lo más probable es que la etiología sea bacteriana.
• Análisis bacteriológico del esputo: no está indicado de forma habitual en las agudizaciones ambulatorias.
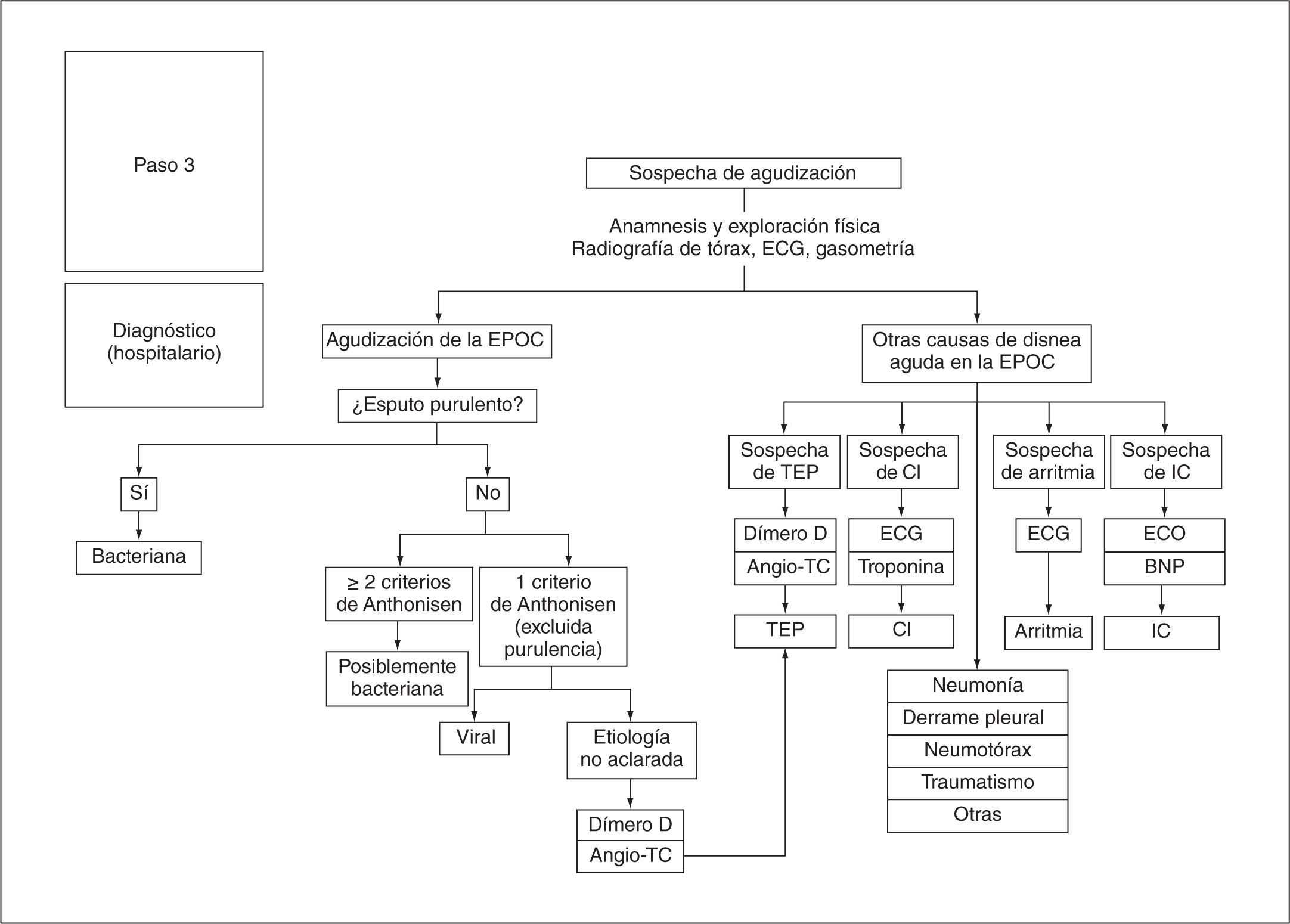
Aproximación diagnóstica hospitalariaA todos los pacientes se les deberá realizar una adecuada historia clínica y una exploración física, como se describe en la agudización ambulatoria. En la figura 5 se recogen las principales pruebas diagnósticas que hay que realizar para caracterizar adecuadamente la agudización hospitalaria.
- •
Historia clínica y exploración física.
- •
Analítica de sangre: debe incluir hemograma y parámetros bioquímicos como glucemia, urea, creatinina y electrolitos.
- •
Gasometría arterial: siempre se deberá recoger la fracción inspiratoria de oxígeno a la que se realiza la técnica. En los pacientes que presenten hipercapnia y/o acidosis inicial deberá realizarse una segunda gasometría de control a los 30-60 min.
- •
Radiografía de tórax.
- •
ECG.
- •
Análisis microbiológico del esputo: se deberá realizar una tinción de Gram y cultivo aerobio. Está indicado en pacientes con frecuentes agudizaciones, en los que presenten fracaso terapéutico o en agudizaciones que precisen ventilación mecánica.
Diagnóstico hospitalario de la etiología de la agudización de la EPOC. Angio-TC: angiografía por tomografía computarizada; BNP: péptido natriurético tipo B; CI: cardiopatía isquémica; ECG: electrocardiograma; ECO: ecocardiografía; IC: insuficiencia cardíaca; TEP: tromboembolia pulmonar.
Tras la valoración inicial, se deberán descartar otras causas de disnea (v. diagnóstico diferencial, tabla 1). La radiografía de tórax y el ECG pueden ser de ayuda para ello. La angiografía por tomografía computarizada (angio-TC) estará indicada en pacientes con sospecha moderada-alta de tromboembolia pulmonar (TEP) y también en las agudizaciones de causa no aclarada.
La determinación de algunos biomarcadores plasmáticos, como el dímero D, la troponina o el péptido natriurético tipo B (BNP), puede ser de utilidad en caso de sospecha de TEP, cardiopatía isquémica o insuficiencia cardíaca, respectivamente. Algunos de estos biomarcadores, como la troponina T o el BNP, pueden estar elevados en agudizaciones de EPOC sin cardiopatía conocida asociada. En estos casos, la elevación de estos biomarcadores se asocia a un peor pronóstico13.
En los casos en que la etiología continúe sin conocerse después de esta valoración inicial, se buscará la posible existencia de una embolia pulmonar y se recomienda la determinación de dímero D y, si este es positivo, de angio-TC. Con probabilidad baja o intermedia, la determinación de dímero D negativa excluye la anticoagulación y la continuación del estudio en búsqueda de TEP26. En una revisión sistemática reciente se ha identificado una prevalencia del 16,1% (IC del 95%, 8,325,8%) de TEP en pacientes con agudización de EPOC de causa no aclarada27.
Las pautas de tratamiento deberán ser las adecuadas para cada paciente en función de la posible etiología de la agudización y de su gravedad. En este sentido, se distinguen 2 escenarios de tratamiento: el ambulatorio y el hospitalario. Más del 80% de las agudizaciones se manejan de forma ambulatoria28.
En todos los casos, el tratamiento broncodilatador destinado al alivio inmediato de los síntomas se considera fundamental, mientras que el uso de antibióticos, corticoides sistémicos, oxigenoterapia, ventilación asistida, rehabilitación pulmonar (RP) o el tratamiento de la propia comorbilidad variarán según las características de la propia agudización. Se deberá valorar la necesidad de tratamiento antibiótico como se ha descrito previamente.
Tratamiento farmacológico de la agudizaciónDiversos aspectos del tratamiento de la agudización de la EPOC han sido analizados recientemente en una normativa conjunta ERS/ ATS29. Algunas de las recomendaciones recogidas en GesEPOC son consistentes con dichas recomendaciones.
BroncodilatadoresEn la agudización de la EPOC, de cualquier intensidad, la principal intervención consiste en la optimización de la broncodilatación, aumentando la dosis y/o la frecuencia de los broncodilatadores30.
Broncodilatadores de acción cortaLos BDCD son los broncodilatadores de elección para el tratamiento de la agudización. Se deberán emplear fármacos de acción corta y rápida, como los agonistas beta-2 (salbutamol y terbutalina), y, si fuera necesario, se pueden añadir al tratamiento los anticolinérgicos de acción corta (ipratropio).
Dispositivos de liberación. Para administrar los fármacos inhalados durante la agudización, se pueden utilizar dispositivos presurizados de dosis medida (pMDI) con cámara de inhalación o nebulizadores. En una revisión sistemática sobre las formas de administración de los BDCD se concluye que cuando la técnica inhalatoria es buena, no hay diferencias significativas sobre el volumen espiratorio forzado en el primer segundo (FEV1) entre los cartuchos presurizados con o sin cámara espaciadora y los nebulizadores31.
La elección del sistema dependerá de la dosis que precise el paciente, de su capacidad para utilizar el dispositivo y de la posibilidad de supervisión de la terapia. Cuando se precisan dosis bajas de medicación (p. ej., 100-400μg de salbutamol) es preferible el pMDI con cámara, mientras que los nebulizadores pueden liberar dosis más elevadas con mayor facilidad. En los casos donde el nivel de colaboración sea insuficiente se podrá utilizar la medicación de forma nebulizada32.
En pacientes con hipercapnia o acidosis, la medicación nebulizada debe ser liberada utilizando dispositivos de aire comprimido y no mediante el uso de oxígeno a alto flujo, ya que esta última forma de administración puede empeorar la hipercapnia.
Dosis. Las dosis recomendadas son para el caso del salbutamol de 400-600μg/4-6 h (4-6 inhalaciones/4-6 h) o terbutalina 500-1.000μg/4-6 h (1-2 inhalaciones/6 h), y en el caso de ipratropio, de 80-120μg/4-6 h (4-6 inhalaciones/4-6 h). En el caso de utilizar la medicación nebulizada, la pauta será de 2,5-10mg de salbutamol y/o 0,5-1mg de ipratropio cada 4-6 h.
Broncodilatadores de larga duraciónLos BDLD constituyen el tratamiento de base de la EPOC y su eficacia en la agudización no está suficientemente documentada33. Sin embargo, es importante recordar que si el paciente ya utiliza BDLD para el control de su enfermedad de base, estos no deberán suspenderse durante el tratamiento de la agudización ambulatoria.
Metilxantinas. Debido a la posible aparición de efectos adversos significativos, las teofilinas no se recomiendan habitualmente para el tratamiento de las agudizaciones de la EPOC. En una revisión sistemática se observó que las metilxantinas en pacientes con EPOC moderada-grave no mejoraron de forma importante el curso clínico de las agudizaciones, mostrando escasos beneficios sobre la función pulmonar (FEV1), con una incidencia significativa de efectos secundarios (náuseas y vómitos)34.
Optimizar el tratamiento de la comorbilidadEn la EPOC es frecuente la coexistencia de distintas comorbilidades, como hipertensión arterial, cardiopatía isquémica, arritmias, insuficiencia cardíaca o diabetes. Por ello será necesario optimizar su tratamiento.
AntibióticosEn general, se recomienda utilizar antibióticos durante una agudización siempre que aparezca un cambio en el color del esputo, como expresión indirecta de posible infección bacteriana. La reciente normativa de la ERS/ATS recomienda el uso ambulatorio de antibióticos, en especial si hay cambios en el color del esputo29.
- •
En la agudización leve estará indicado el uso de antibióticos en presencia de esputo purulento22,35,36.
- •
En la agudización moderada o grave, también estará indicado cuando, en ausencia de purulencia, exista incremento de la disnea y del volumen del esputo.
- •
En las agudizaciones muy graves, cuando el paciente requiere asistencia ventilatoria, la cobertura antibiótica es obligada, ya que ha demostrado reducir la incidencia de neumonía secundaria y también reducir de forma significativa la mortalidad37a.
P17. En los pacientes con EPOC, ¿se recomienda el uso de antibióticos en el tratamiento ambulatorio de las agudizaciones?
Recomendación débil a favor. En un contexto de atención ambulatoria, en los pacientes con exacerbación de la EPOC con sospecha de infección, definida por la presencia de esputo purulento o cambios en el color del esputo, se sugiere la administración de antibióticos orales.
Especificaciones. La selección del antibiótico debe considerar los patrones de resistencia locales a los patógenos más comunes. En exacerbaciones leves o moderadas, la presencia de un esputo purulento o cambio en el color del esputo se pueden considerar como indicadores de infección. La gravedad de la enfermedad de base es un factor que puede aconsejar el tratamiento antibiótico.
Elección del antibióticoLa tabla 6 indica cuáles son los principales antibióticos que se pueden utilizar durante una agudización de la EPOC. Esta elección dependerá del conocimiento de las especies bacterianas involucradas, resistencias antibióticas locales, la gravedad de la propia agudización y del riesgo de infección por P. aeruginosa. Este riego se define por el uso de más de 4 ciclos de tratamiento antibiótico en el último año, una función pulmonar con un FEV1 < 50% del predicho, la presencia de bronquiectasias significativas o el aislamiento previo de Pseudomonas en esputo en fase estable o en una agudización previa37b.
Recomendación sobre el uso de antibióticos en la agudización de la EPOC
| Gravedad de la agudización | Gérmenes | Antibiótico de elección | Alternativas |
|---|---|---|---|
| Agudización leve | Haemophilus influenzae Streptococcus pneumoniae Moraxella catarrhalis | Amoxicilina-ácido clavulánico | Cefditoren Moxifloxacino Levofloxacino |
| Agudización moderada | Igual que grupo A + S. pneumoniae resistente a penicilina Enterobacterias | Moxifloxacino Levofloxacino | Amoxicilina-ácido clavulánico |
| Agudización grave-muy grave sin riesgo de infección por Pseudomona | Igual que grupo B | Moxifloxacino Levofloxacino | Amoxicilina-ácido clavulánico Ceftriaxona Cefotaxima |
| Agudización grave-muy grave con riesgo de infección por Pseudomonas | Igual que grupo B + Pseudomonas aeruginosa | Ciprofloxacino Levofloxacino a dosis altasa | Betalactamasa con actividad anti-Pseudomonasb |
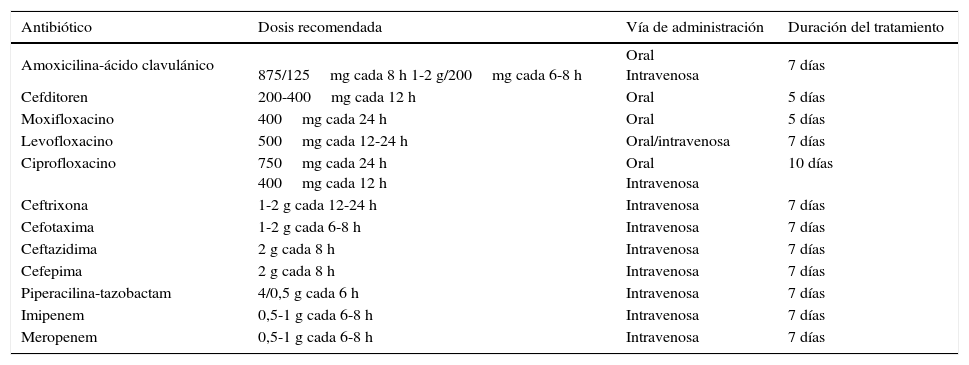
En la tabla 7 se recogen las dosis recomendadas de cada fármaco, la vía de administración y su duración de acción.
Dosis recomendada, vía de administración y duración de los principales antibióticos
| Antibiótico | Dosis recomendada | Vía de administración | Duración del tratamiento |
|---|---|---|---|
| Amoxicilina-ácido clavulánico | 875/125mg cada 8 h 1-2 g/200mg cada 6-8 h | Oral Intravenosa | 7 días |
| Cefditoren | 200-400mg cada 12 h | Oral | 5 días |
| Moxifloxacino | 400mg cada 24 h | Oral | 5 días |
| Levofloxacino | 500mg cada 12-24 h | Oral/intravenosa | 7 días |
| Ciprofloxacino | 750mg cada 24 h 400mg cada 12 h | Oral Intravenosa | 10 días |
| Ceftrixona | 1-2 g cada 12-24 h | Intravenosa | 7 días |
| Cefotaxima | 1-2 g cada 6-8 h | Intravenosa | 7 días |
| Ceftazidima | 2 g cada 8 h | Intravenosa | 7 días |
| Cefepima | 2 g cada 8 h | Intravenosa | 7 días |
| Piperacilina-tazobactam | 4/0,5 g cada 6 h | Intravenosa | 7 días |
| Imipenem | 0,5-1 g cada 6-8 h | Intravenosa | 7 días |
| Meropenem | 0,5-1 g cada 6-8 h | Intravenosa | 7 días |
En varios ensayos clínicos aleatorizados38–40 se ha evaluado la utilidad de la budesonida nebulizada a dosis altas (2mg, 3 o 4 veces al día) frente a placebo en pacientes con EPOC hospitalizados por agudización moderada-grave no acidótica y han demostrado mejoría del FEV1 tras broncodilatación y de la PaO2 (presión arterial de oxígeno). En ambos casos se ha demostrado que este tratamiento puede ser una alternativa eficaz y segura, aunque más cara, a los corticoides orales cuando se produce una exacerbación de la EPOC.
Profilaxis de la enfermedad tromboembólica venosaLas agudizaciones graves o muy graves de la EPOC comportan un riesgo alto de enfermedad tromboembólica venosa, por lo que se recomienda el uso de heparinas de bajo peso molecular a dosis moderadas41. En las agudizaciones moderadas, en las que el paciente permanece encamado o inactivo, también está indicado su uso.
Tratamiento del tabaquismo durante la agudizaciónEl abandono del tabaco es una medida deseable en cualquier momento de la evolución de la EPOC. En este sentido, se sugiere iniciar la terapia de deshabituación aprovechando el proceso de agudización de la EPOC.
P18. En los pacientes con EPOC hospitalizados, ¿se recomienda realizar tratamientos de deshabituación tabáquica en un contexto de agudización de la EPOC respecto al tratamiento habitual?
Recomendación débil a favor. De ser posible se sugiere iniciar la terapia de deshabituación tabáquica durante la hospitalización por agudización de la EPOC.
Especificaciones. En los ámbitos donde existe un programa de deshabituación establecido, se debe verificar que la intervención se dé de forma intensiva y tenga un seguimiento de apoyo de al menos 1 mes tras el alta.
Corticoides sistémicosLos corticoides sistémicos han demostrado acelerar la recuperación de los síntomas, mejorar la función pulmonar y disminuir los fracasos terapéuticos42. En las agudizaciones moderadas y en las graves-muy graves deberá emplearse una tanda corta de corticoides sistémicos durante 5 días43. También se valorará el uso de estos fármacos en los pacientes con agudizaciones leves que no responden satisfactoriamente al tratamiento inicial. Estudios recientes indican que los corticoides pueden ser menos eficaces en pacientes con cifras bajas de eosinófilos en sangre15. La normativa ERS/ATS recomienda el uso de tandas cortas de corticosteroides orales en las agudizaciones ambulatorias que cursan con disnea importante29.
Dosis, duración y vía de administraciónSe recomienda administrar 0,5mg/kg/día por vía oral (máximo de 40mg/día) de prednisona o equivalentes durante 5 días43. En pacientes con EPOC hospitalizados por una exacerbación que no precisen ventilación mecánica, se sugiere utilizar también la vía oral.
En la mayoría de los estudios, las tandas cortas de corticoides sistémicos se interrumpen de forma brusca, sin que se produzcan efectos secundarios. La reducción progresiva de la dosis de corticoides no ha sido estudiada.
P19. En los pacientes con EPOC hospitalizados, ¿se recomienda administrar corticoides por vía intravenosa frente a corticoides por vía oral para el tratamiento de las exacerbaciones?
Recomendación débil en contra. En pacientes con EPOC hospitalizados por una exacerbación que toleren la vía oral y que requieran la administración de corticoides sistémicos, se sugiere utilizar preferentemente la vía oral.
Especificaciones. Los estudios excluyeron a los pacientes más graves, con necesidad de ventilación mecánica, pH < 7,26 o hipercápnicos (PaCO2 > 70 mmHg).
Tratamiento no farmacológico de la agudizaciónOxigenoterapiaLa administración de oxígeno suplementario se considera una de las piezas clave del tratamiento de la agudización grave de la EPOC que cursa con insuficiencia respiratoria. El objetivo de la oxigenoterapia es alcanzar una SaO2 entre 88-92% para prevenir la hipoxemia de amenaza vital y optimizar la liberación de oxígeno a los tejidos periféricos. Sin embargo, en los pacientes con EPOC, la administración de oxígeno debe realizarse de forma controlada, ya que en algunos pacientes el principal estímulo del centro respiratorio depende del grado de hipoxemia más que del habitual estímulo hipercápnico. La administración de oxígeno de forma incontrolada puede producir supresión del estímulo respiratorio, carbonarcosis e incluso parada respiratoria.
En la práctica clínica se deben administrar bajas concentraciones inspiratorias de oxígeno (del 24 o el 28%) mediante mascarillas de alto flujo tipo Venturi o mediante gafas nasales a bajos flujos de 2-4 l/min.
Un estudio reciente demuestra que los niveles de bicarbonato y pH medidos en sangre venosa son parecidos a los que se obtienen en sangre arterial44, lo que podría ser de utilidad para evitar gasometrías arteriales, siempre más dificultosas y molestas. Sin embargo, se necesitan datos adicionales para establecer la utilidad precisa de la sangre venosa en el contexto de la insuficiencia respiratoria. Los valores de PaCO2 no son concordantes entre ambos tipos de muestras sanguíneas44.
Durante las agudizaciones graves o muy graves se deberá realizar una gasometría arterial, antes y después de iniciar el tratamiento suplementario con oxígeno, especialmente si cursan con hipercapnia.
Rehabilitación pulmonar precozEn pacientes hospitalizados por una agudización de EPOC, los programas de RP temprana reducen los reingresos y mejoran la CVRS y la capacidad de ejercicio45. No obstante, estos resultados son variables según el momento de inicio del programa. La disminución de reingresos únicamente es significativa para programas iniciados tras el alta hospitalaria (hasta 3 semanas después del alta). Adicionalmente, se ha observado una tendencia al aumento de la mortalidad asociada a RP que es estadísticamente significativa en los programas iniciados durante el ingreso. Este efecto se observó en los resultados obtenidos en un ensayo realizado en el Reino Unido46, aunque —debido al escaso número de eventos— no se puede descartar que se trate de un efecto espurio.
P21. En los pacientes con EPOC hospitalizados por exacerbación de la EPOC, ¿se recomienda la rehabilitación pulmonar temprana frente a la atención habitual?
Recomendación débil a favor. Se sugiere iniciar un programa de RP tras el alta en los pacientes que han sido hospitalizados por una exacerbación de la EPOC.
Especificaciones. El grupo de elaboración de la guía considera que los programas de RP en los pacientes que han presentado una agudización grave (que ha requerido ingreso hospitalario) pueden ser beneficiosos para mejorar la capacidad funcional, reducir futuros ingresos hospitalarios y mejorar la CVRS de estos pacientes. El clínico debe valorar la disponibilidad de programas de RP en su entorno sanitario y si es factible que el paciente los pueda cumplir correctamente. Todavía hay dudas acerca del momento idóneo para iniciar un programa de rehabilitación y, hasta que no se disponga de información más fiable, se debería evitar el inicio de la RP durante el ingreso hospitalario.
Ventilación asistidaEn los casos donde existe un fracaso ventilatorio grave, con alteración del nivel de consciencia, disnea invalidante o acidosis respiratoria, a pesar de tratamiento médico optimo, se debe considerar el empleo de soporte ventilatorio. Se puede administrar como VMNI o como ventilación mecánica invasiva (VMI).
Ventilación mecánica no invasivaInstaurar la VMNI en pacientes hospitalizados con fallo respiratorio agudo hipercápnico disminuye la mortalidad, la necesidad de intubación y las complicaciones del tratamiento respecto al tratamiento habitual sin soporte ventilatorio. También disminuye la estancia hospitalaria y la estancia en la unidad de cuidados intensivos47. La tabla 8 señala cuáles son las indicaciones y contraindicaciones de la VMNI.
Indicaciones y contraindicaciones relativas de la ventilación mecánica no invasiva
| Indicaciones |
| • Acidosis respiratoria (pH < 7,35) con hipercapnia (PaCO2 > 45 mmHg) a pesar de tratamiento óptimo |
| Contraindicaciones |
| • Parada respiratoria |
| • Inestabilidad cardiovascular |
| • Somnolencia que impida la colaboración del paciente |
| • Alto riesgo de aspiración |
| • Cirugía facial o gastroesofágica reciente |
| • Anomalías nasofaríngeas |
| • Quemados |
PaCO2: presión arterial de dióxido de carbono.
P22. En los pacientes hospitalizados con una exacerbación de la EPOC, ¿se recomienda el uso de la ventilación no invasiva frente a la atención habitual?
Recomendación fuerte a favor. Se recomienda iniciar la ventilación no invasiva en pacientes con EPOC que cursan con insuficiencia respiratoria hipercápnica y acidosis respiratoria moderada a pesar de tratamiento médico óptimo.
Especificaciones. El grupo elaborador considera razonable definir insuficiencia respiratoria con hipercapnia si la PaCO2 es superior a 45 mmHg y acidosis cuando el pH es inferior a 7,35. Se deben considerar como contraindicaciones formales de la VMNI los trastornos del nivel de consciencia o somnolencia, alto riesgo de aspiración, malformaciones nasofaríngeas, uso de musculatura accesoria por disnea grave, o inestabilidad cardiovascular. El grupo elaborador considera que el seguimiento de los parámetros gasométricos antes y durante la VMNI es una buena práctica clínica
Ventilación mecánica invasivaLa VMI debe considerarse en los casos donde se produzca acidemia y/o hipoxemia grave, junto con deterioro del estado mental48. Tradicionalmente se ha asumido que los pacientes con EPOC que precisan VMI presentaban cifras de mortalidad muy elevadas, por lo que en muchas ocasiones su indicación podría ser controvertida. Sin embargo, datos consistentes refieren que la mortalidad observada se sitúa alrededor del 20%, una cifra incluso inferior a la observada para otras patologías tratadas con VMI. En la tabla 9 se muestran las indicaciones absolutas y relativas de la VMI.
Indicaciones absolutas y relativas de la ventilación mecánica invasiva
| Indicaciones absolutas |
| • Parada respiratoria |
| • Fracaso de la VMNI o presencia de criterios de exclusión |
| • Hipoxemia grave (PaO2 < 40 mmHg) a pesar de tratamiento correcto |
| • Empeoramiento de la acidosis respiratoria (pH < 7,25) a pesar de tratamiento correcto |
| • Disminución del nivel de consciencia o confusión que no mejora con tratamiento |
| Indicaciones relativas |
| • Disnea grave con uso de musculatura accesoria |
| • Complicaciones cardiovasculares (hipotensión, shock, etc.) |
PaO2: presión arterial de oxígeno; VMNI: ventilación mecánica no invasiva
Si el paciente no recibía tratamiento previo, se deberá pautar un tratamiento adecuado para la fase estable de la enfermedad, de acuerdo con su nivel de riesgo y fenotipo específico.
SeguimientoPara las agudizaciones ambulatorias se establece un control evolutivo con una visita a las 72 h del inicio del tratamiento, en el ámbito de atención primaria, con la intención de valorar la evolución del proceso de agudización. Este período es importante para poder identificar la existencia de fracasos terapéuticos precoces. En el caso de que el paciente haya precisado ingreso hospitalario, el control evolutivo inicial deberá realizarse dentro de las 2 primeras semanas tras el alta hospitalaria y es aconsejable una visita adicional a las 8-12 semanas.
Según el estudio AUDIPOC49 —una auditoria clínica realizada en 129 hospitales españoles— la mortalidad global a los 90 días tras una hospitalización por agudización de EPOC fue del 11,6%, aunque con variaciones que oscilaron entre el 0 y el 50%. La tasa de reingresos fue del 37% y también presentó fuertes variaciones, entre el 0 y el 62%. Estos datos refuerzan la necesidad de un seguimiento cercano que reduzca la variabilidad y minimice las consecuencias.
En la primera consulta se evaluarán la situación clínica y la respuesta terapéutica; se detectarán los casos con dificultad para la comprensión de las indicaciones y aquellas situaciones de riesgo especial, y se revisarán aspectos diagnósticos, de adherencia y tolerancia del tratamiento. Asimismo, se insistirá en aspectos educativos y preventivos y se potenciará la implicación de los pacientes y cuidadores en aspectos de autocuidado.
Se recomienda efectuar una visita de seguimiento adicional a las 8-12 semanas para asegurar que el paciente ha retornado a la estabilidad. En esta visita se deben revisar sus síntomas, reclasificar el riesgo, el fenotipo clínico, la adherencia al tratamiento, los aspectos educativos y/o el ajuste del tratamiento preventivo50. Los pacientes que hayan precisado oxigenoterapia durante la exacerbación previa se deberán revaluar para valorar la indicación de oxigenoterapia continua domiciliaria.
En todos los pacientes que no dispongan de espirometría previa, se etiquetará el caso como “Posible EPOC”. Se deberá realizar una espirometría de confirmación en fase de estabilidad.
Criterios de valoración hospitalariaEn función de la gravedad de la agudización, el paciente deberá recibir asistencia ambulatoria u hospitalaria. En la tabla 10 se recogen los criterios que se deben considerar para remitir al paciente al hospital en el transcurso de una agudización.
Indicaciones para remitir al paciente a valoración hospitalaria
| Agudización grave o muy grave |
| • Disnea 3-4 de la escala mMRC |
| • Inestabilidad hemodinámica |
| • Alteración del nivel de consciencia |
| • Cianosis de nueva aparición |
| • Utilización de musculatura accesoria |
| • Edemas periféricos de nueva aparición |
| • SpO2 < 90% o PaO2 < 60 mmHg |
| • Comorbilidad significativa grave* |
| • Complicaciones (arritmias graves, insuficiencia cardíaca, etc.) |
| Fracaso terapéutico en las agudizaciones moderadas (falta de respuesta al tratamiento) |
| Pacientes con EPOC estable graves/muy graves y agudizaciones frecuentes (≥ 2) en el año previo |
| Descartar otros diagnósticos (neumonía, neumotórax, insuficiencia cardíaca, embolia pulmonar, etc.) |
| Apoyo domiciliario insuficiente Deterioro del estado general |
mMRC: escala de disnea modificada de la Medical Research Council; PaO2: presión arterial de oxígeno; SpO2: saturación parcial de oxígeno.
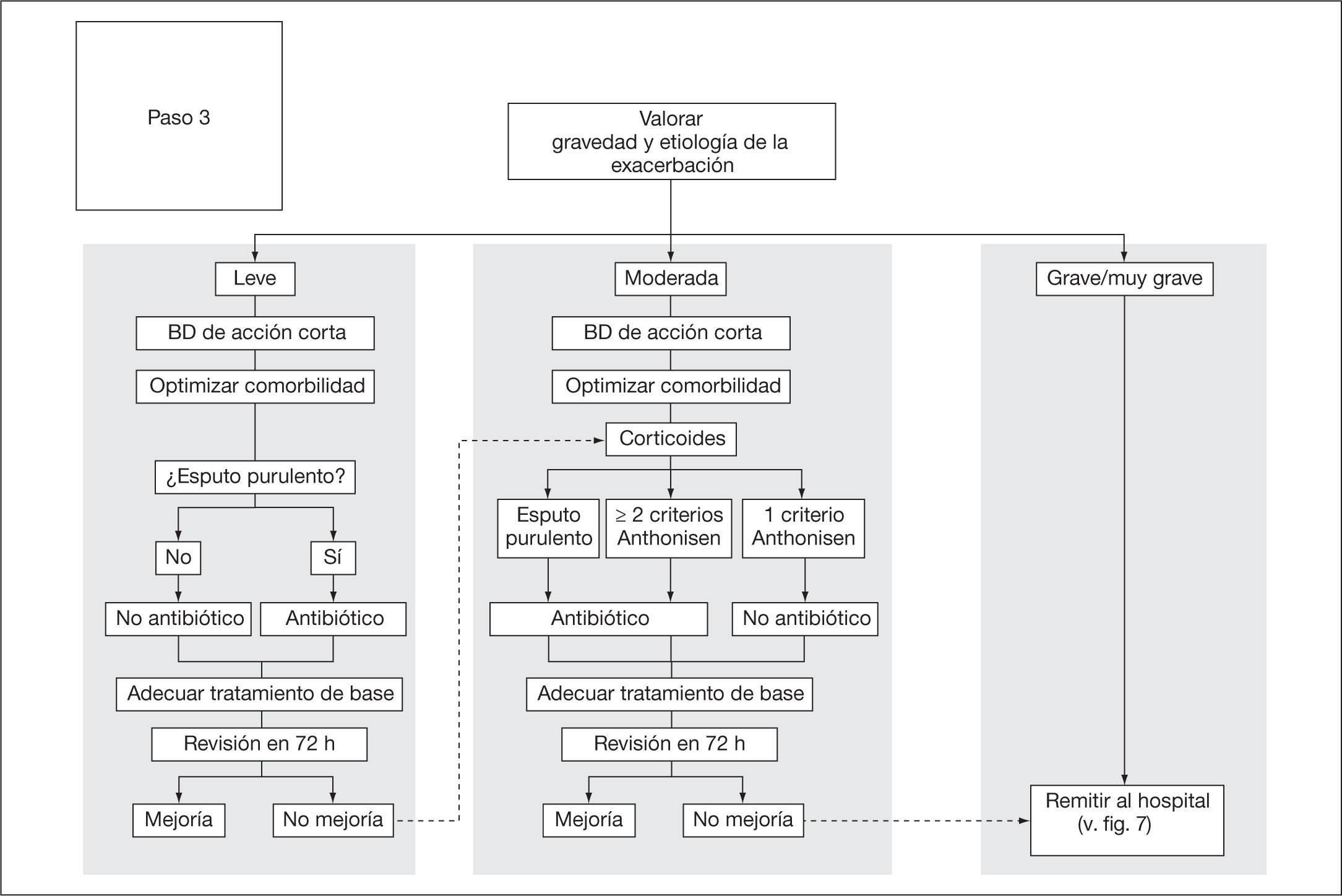
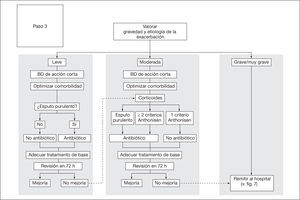
En la figura 6 se expone el esquema terapéutico que se recomienda en pacientes con agudizaciones leves y moderadas. Los pacientes que cumplan criterios de agudización grave o muy grave deberán remitirse al hospital.
Aunque hay pautas terapéuticas comunes, la intensidad del tratamiento administrado dependerá de la gravedad de la propia agudización. La principal diferencia entre las agudizaciones leves y moderadas se encuentra en el uso de corticoides sistémicos, recomendados para las agudizaciones moderadas. La pauta antibiótica dependerá de la sospecha de infección bacteriana. No obstante, mientras en la agudización leve se exige un cambio en la coloración del esputo (amarillento, verdoso o amarronado), en la moderada podría pautarse antibiótico también en los casos donde —además de la disnea— aparece aumento de volumen del esputo, aunque no haya cambios en su color.
Algoritmo terapéutico hospitalario de la agudización de la EPOCAunque el esquema terapéutico para todas las agudizaciones graves o muy graves es similar, la estructura y organización de la asistencia será diferente según el lugar donde se atienda al paciente: servicio de urgencias, sala de hospitalización o unidad especializadas de cuidados intermedios o de cuidados intensivos. Las recomendaciones para la atención al paciente en unidades de críticos no se recogen en esta guía.
Asistencia en el servicio de urgencias hospitalariasLa asistencia al paciente con agudización de EPOC en el servicio de urgencias hospitalarias debe estar estructurada en 4 fases:
- •
Fase 1: admisión y clasificación.
- •
Fase 2: asistencia.
- •
Fase 3: evolución, espera y observación.
- •
Fase 4: resolución, orientación y transferencia.
Ante todo paciente que consulte en urgencias hospitalarias, lo primero que se debe hacer es realizar una clasificación con un sistema de cribado estructurado y validado. La base fundamental de cualquier sistema de cribado hospitalario moderno es el establecimiento de niveles o categorías en función de los síntomas que expresa el paciente y los signos observados. Los sistemas de cribado no se diseñan para realizar diagnósticos médicos, que son el resultado final de la asistencia, sino para conseguir una clasificación y priorización en la asistencia médica de los servicios de urgencia hospitalarios, y, así, conseguir una adecuación de los recursos disponibles según el nivel de gravedad de cada paciente en particular.
Clasificación de prioridad asistencialEl Sistema Español de Triaje (SET) establece cinco niveles de priorización (tabla 11), a partir de la combinación de las siguientes circunstancias:
Niveles de priorización para la asistencia en el servicio de urgencias de la agudización de la EPOC según el Sistema Español de Triaje
| Nivel | Recomendación | Recomendación | Tiempo de atención de enfermería | Tiempo de atención del facultativo |
|---|---|---|---|---|
| I | Se adjudica a los pacientes que requieren resucitación, con riesgo vital inmediato | Disnea clase V (pre-parada respiratoria) Situación de shock | Inmediato | Inmediato |
| II | Pacientes en situación de emergencia o muy urgentes, de riesgo vital inmediato y cuya intervención depende radicalmente del tiempo, son situaciones de alto riesgo, con inestabilidad fisiológica o dolor intenso | Disnea clase IV (muy grave) Estridor > 2 constantes o signos vitales alterados | Inmediato | 5-15 min |
| III | Lo constituyen las situaciones urgentes, de riesgo potencial, que generalmente requieren múltiples exploraciones diagnósticas y/o terapéuticas en pacientes con estabilidad fisiológica (constantes vitales normales) | Disnea de clase III (grave) Estabilidad hemodinámica Síntomas y signos de insuficiencia respiratoria | 30 min | 15-60 min |
| IV | Son situaciones menos urgentes, potencialmente serias y de una complejidad-urgencia significativa. Suelen necesitar una exploración diagnóstica y/o terapéutica | Disnea clase I-II (leve-moderada) Estabilidad hemodinámica Sin insuficiencia respiratoria | 60 min | 30-120 min |
| V | Son situaciones no urgentes que generalmente no requieren ninguna exploración diagnóstica y/o terapéutica | 120 min | 40-240 min |
1. Categorización sintomática. En un paciente con una agudización de EPOC, el síntoma guía principal que le llevará a un servicio de urgencias hospitalario, en la gran mayoría de los casos, es el incremento de su disnea.
En la categoría sintomática disnea se aplican inicialmente los algoritmos y/o escalas de valoración globales que determinan el riesgo vital del paciente en base a los parámetros de sus constantes vitales. Esta valoración general puede determinar por sí misma un nivel I de prioridad si encuentra inestabilidad hemodinámica.
2. Valoración de los signos y síntomas. Las constantes y signos vitales alterados en el adulto discriminarán los pacientes entre el nivel II y III. Es decir, que 2 pacientes con idéntica sintomatología y situación clínica serán discriminados a nivel II si tienen las constantes o signos vitales alterados.
El SET considera constantes vitales alteradas en el adulto, 2 o más de las siguientes:
- •
Presión arterial sistólica < 90 o ≥ 200 mmHg.
- •
Frecuencia cardíaca ≤ 40 o ≥ 125 lat/min.
- •
Frecuencia respiratoria ≤ 10 o ≥ 30 resp/min.
- •
SO2 < 92%.
- •
Temperatura corporal < 35,5 o > 40 °C.
- •
Glucemia capilar < 40mg/dl.
- •
Glasgow ≤ 14.
Se consideran signos vitales alterados en el adulto:
- •
Piel fría y pálida, o sudada y caliente o muy caliente.
- •
Falta de pulso radial, pulso débil o pulso muy fuerte.
- •
Pulso muy lento o muy rápido.
- •
Respiración lenta y profunda o superficial y rápida.
- •
Somnolencia o confusión.
3. Escala de gravedad. La categoría disnea en el SET se evalúa de la siguiente forma:
- •
Clase I (leve): ausencia de síntomas con la actividad normal. Equivale a disnea 0 o 1 en la escala mMRC.
- •
Clase II (moderada): síntomas con la actividad moderada. Equivale a disnea 2 en la escala mMRC.
- •
Clase III (grave): síntomas con escasa actividad. Equivale a disnea 3 en la escala mMRC.
- •
Clase IV (muy grave): síntomas en reposo. Equivale a disnea 4 en la escala mMRC.
- •
Clase V (pre-parada respiratoria).
De acuerdo con esta clasificación del SET, y también atendiendo a los criterios de gravedad de la propia agudización (tabla 11), de la presencia de insuficiencia respiratoria y/o de comorbilidad grave, se establecen 3 códigos asistenciales iniciales dentro del servicio de urgencias:
• Código I (amenaza vital): el paciente es candidato a recibir atención en una unidad de cuidados intensivos (tabla 12). Los criterios para el traslado inicial a esta unidad son:
- –
Pacientes en nivel I del SET.
- –
Pacientes en nivel II del SET que además cumplan criterios de ingreso en intensivos.
Indicaciones de ingreso en unidad de cuidados intensivos
| Agudización muy grave |
| • Parada respiratoria |
| • Alteración del nivel de consciencia (confusión, letargia o coma) |
| • Inestabilidad hemodinámica |
| • Acidosis respiratoria grave (pH < 7,30) |
| Disnea grave que no responde al tratamiento inicial |
| Hipoxemia grave, a pesar de tratamiento (PaO2 < 40 mmHg) |
| Hipercapnia o acidosis respiratoria (pH < 7,25) a pesar de ventilación no invasiva |
| Necesidad de ventilación mecánica invasiva |
PaO2: presión arterial de oxígeno.
• Código II (insuficiencia respiratoria sin amenaza vital): el paciente deberá ser atendido en una cama de observación.
- –
Pacientes en nivel II del SET que no cumplan criterios de ingreso en intensivos.
- –
• Código III (sin insuficiencia respiratoria): se podrá atender en el mismo box de urgencias.
- –
Pacientes en nivel IV y V del SET.
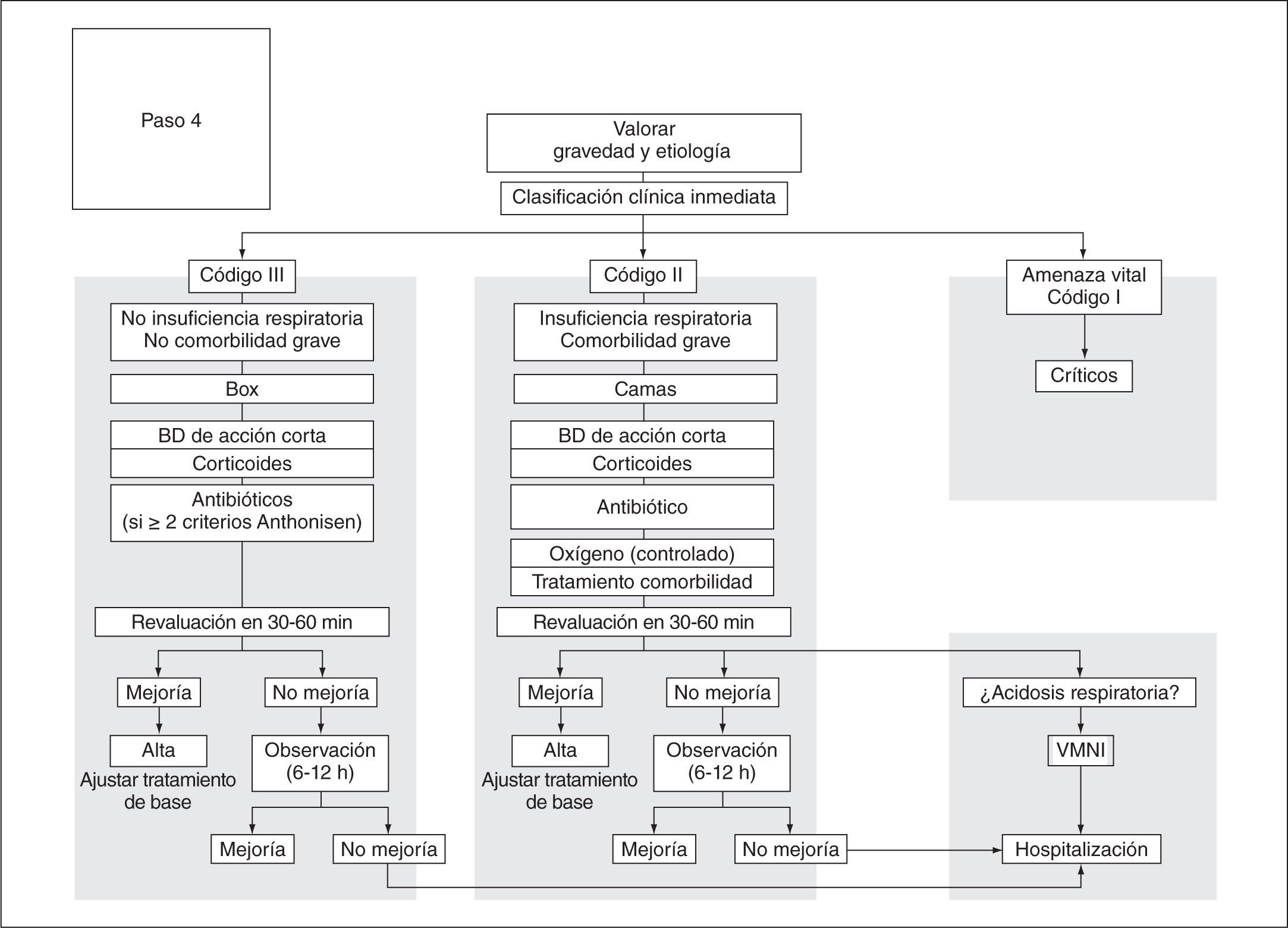
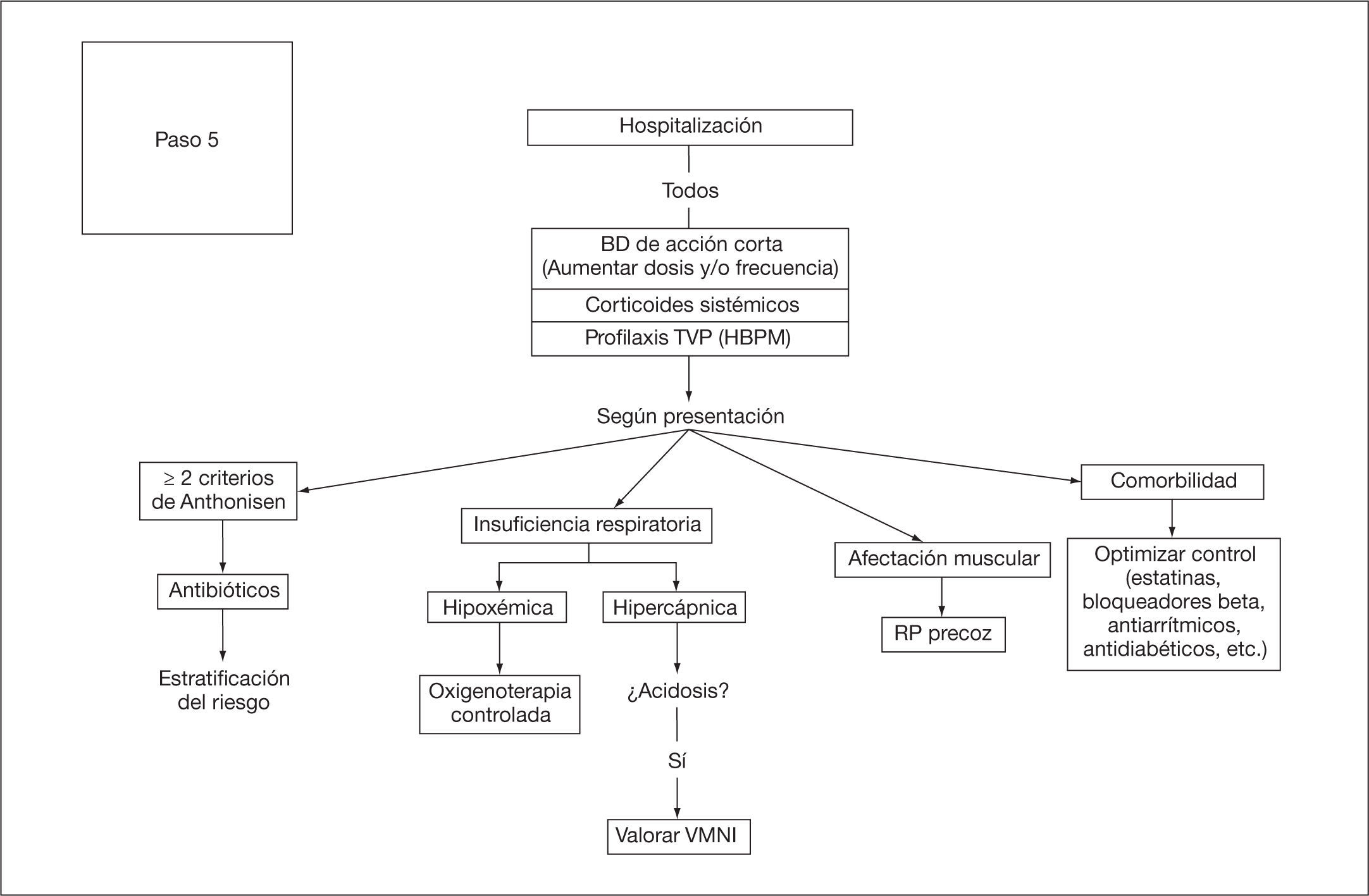
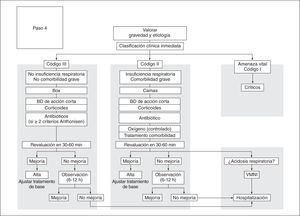
En la figura 7 se muestra el esquema terapéutico que se recomienda en pacientes con agudizaciones graves o muy graves atendidas en el hospital. En ocasiones, pacientes con agudizaciones más leves también acuden a un centro hospitalario. En este último caso, se recomienda seguir el esquema planteado para la agudización ambulatoria.
Los pacientes que cumplan criterios de código I (amenaza vital) deberán ser trasladados al box de críticos para el inicio inmediato del tratamiento. Los casos en los que no se produce una adecuada respuesta y en todos los que cumplan criterios específicos deberán ser trasladados a una unidad de cuidados intensivos (tabla 12). En cuanto a los clasificados como código II y III, el tratamiento será muy similar, con broncodilatadores de acción corta y rápida, corticoides sistémicos y antibióticos, siempre que estén indicados. No obstante, los pacientes con código II deberán ser atendidos en camas de observación, ya que con frecuencia precisan oxigenoterapia controlada y/o tratamiento específico de comorbilidades graves (arritmias, insuficiencia cardíaca, etc.).
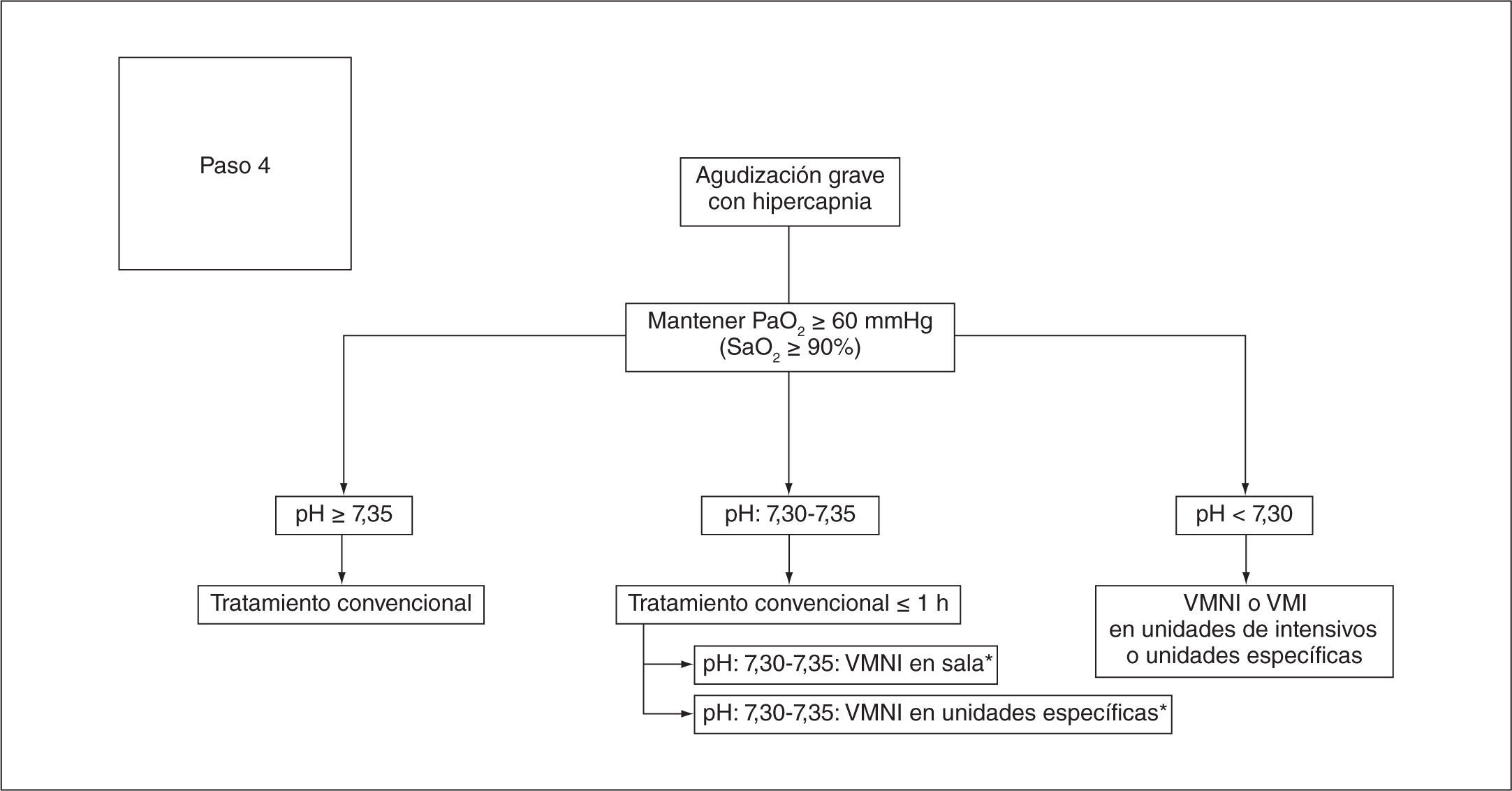
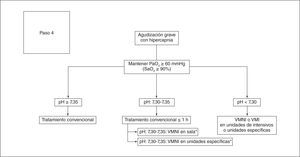
Fase 3. Evolución, espera y observaciónTras el tratamiento inicial, se aconseja una revaluación a los 30-60 min. Si el paciente presentaba una hipercapnia inicial o acidosis, se deberá repetir la gasometría arterial para valorar la indicación de VMNI (fig. 8). Se aconseja iniciar la VMNI de forma precoz, antes de las 4 h.
Se debe optimizar el tratamiento y mantener al paciente en la sala de observación durante un intervalo de tiempo de 6-12 h hasta decidir su destino.
Fase 4. Resolución, orientación y transferenciaAlta domiciliariaLos pacientes que respondan favorablemente al tratamiento y cumplan los criterios de derivación domiciliaria podrán ser dados de alta. En este momento será muy importante adecuar el tratamiento de base para reducir fracasos terapéuticos, recaídas o recurrencias. Asimismo, se deberá realizar un control clínico en un plazo de 72 h. Para ello deben establecerse en cada territorio programas o protocolos destinados a asegurar esta continuidad asistencial.
En todos los pacientes que no dispongan de espirometría previa, se etiquetará el caso como “Posible EPOC”. Se deberá realizar una espirometría de confirmación en fase de estabilidad.
Hospitalización a domicilioLa hospitalización a domicilio representa una alternativa asistencial para pacientes con EPOC que experimentan exacerbaciones sin presentar acidosis. Este tipo de aproximaciones son seguras si se comparan con la hospitalización convencional. Los pacientes con alteraciones del estado mental, cambios radiológicos o electrocardiográficos agudos, necesidades de VMI, comorbilidades significativas y bajo apoyo social no deben incluirse en estos programas.
P20. En los pacientes con un episodio de exacerbación de la EPOC, ¿se recomienda la hospitalización a domicilio como alternativa a la atención convencional?
Recomendación débil a favor. En aquellos centros en los que ya se dispone de una estructura de hospitalización a domicilio se sugiere ofrecer esta opción a los pacientes que requieren una atención hospitalaría urgente por una exacerbación de la EPOC no acidótica. Se ofrecerá tras una valoración clínica y siempre que se cuente con un adecuado soporte familiar o social en el entorno del paciente.
Especificaciones. En la mayoría de estudios se excluyó a los pacientes con alteraciones del nivel de consciencia, alteraciones del equilibrio ácido-base, cambios agudos en el patrón radiológico, necesidades VMI y/o patologías concomitantes graves o mal controladas (como demencia, cáncer, fallo renal, diabetes o hipertensión). Sin embargo, puede haber otros factores, por lo que la decisión de recomendar una hospitalización a domicilio debe ser individualizada y aceptada por los pacientes y cuidadores.
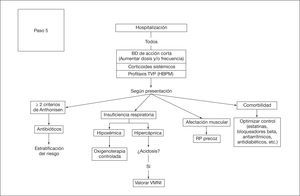
Ingreso hospitalario en sala de hospitalizaciónEn la tabla 13 se exponen los criterios de ingreso hospitalario. Para los casos en que finalmente se requiera un ingreso hospitalario, la figura 9 muestra la pauta de tratamiento que se debe seguir. En pacientes de edad avanzada y comorbilidad (habitualmente código II) que, sin estar en situación crítica, se considere que un ingreso prolongado puede comportar riesgo y se prevea una posible mejoría en 48-72 h, debe considerarse el ingreso en unidades médicas de corta estancia en los hospitales en los que existan. También pueden ser candidatos al ingreso en este tipo de unidades los pacientes que inicialmente presenten criterios de derivación a hospitalización a domicilio y que no reúnan las condiciones psicosociales y/o familiares para ello.
Criterios de ingreso hospitalario en sala de hospitalización
| Ausencia de mejoría tras tratamiento correcto y observación de 6-12 h Acidosis respiratoria (pH < 7,35) |
| PaO2 < 55 mmHg |
| PaCO2 > 50 mmHg en pacientes sin hipercapnia previa |
| Necesidad de ventilación mecánica no invasiva |
| Presencia de complicaciones o comorbilidades graves: |
| • Neumonía, siempre que se cumplan los criterios específicos de gravedad de la neumonía que indican ingreso. |
| • Derrame pleural |
| • Neumotórax |
| • Enfermedad venosa tromboembólica |
| • Traumatismo torácico con fracturas costales |
| • Alteraciones cardiovasculares (insuficiencia cardíaca, cardiopatía isquémica, arritmias no controladas) |
| • Anemia grave |
| Soporte domiciliario insuficiente |
PaCO2: presión arterial de dióxido de carbono; PaO2: presión arterial de oxígeno.
La duración de la estancia hospitalaria es variable de unos pacientes a otros, y no existen suficientes datos para establecer la duración óptima de la hospitalización en pacientes individuales con agudización de EPOC. En la tabla 14 se exponen los criterios que se deben cumplir para proceder al alta hospitalaria.
Criterios de alta hospitalaria
| La administración de broncodilatadores de acción corta no se precisa con una frecuencia inferior a las 4 h |
| El paciente es capaz de caminar por la habitación |
| El paciente es capaz de comer y dormir sin frecuentes despertares debidos a la disnea |
| Estabilidad clínica de 12-24 h |
| Estabilidad gasométrica durante 12-24 h |
| Correcto uso de la medicación por parte del paciente y/o del cuidador |
| Garantía de la continuidad asistencial |
Siempre que se produzca el alta hospitalaria, se deberá adecuar el tratamiento de base, con especial énfasis en reducir las posibles recaídas. En la tabla 15 se recogen las principales recomendaciones terapéuticas para el alta hospitalaria.
Recomendaciones de tratamiento al alta hospitalaria
| Abstinencia tabáquica |
| Recomendación de ejercicio regular. Valorar RP tras hospitalización Mantener y ajustar el tratamiento habitual: |
| • Revisar la técnica inhalatoria del paciente |
| • Broncodilatadores de larga duración de base |
| • Corticoides inhalados: indicados para pacientes con fenotipo agudizador o mixto. |
| • Inhibidores de fosfodiesterasa 4: indicados para fenotipo agudizador con bronquitis crónica |
| • Oxigenoterapia: reajustar según necesidades |
| Antibióticos si se cumplen las indicaciones |
| Corticoides orales: 30-40mg de prednisolona o el equivalente durante 5 días VMNI domiciliaria. Considerarla en pacientes con agudizaciones acidóticas recurrentes y/o en paciente que asocien hipoventilación por otras causas (síndrome de apnea-hipoapnea, obesidad-hipoventilación, etc.) |
| Control clínico en 2-4 semanas |
| Asegurar el correcto cumplimiento |
| Planificación de cuidados de enfermería |
| Garantizar la continuidad asistencial |
RP: rehabilitación pulmonar; VMNI: ventilación mecánica no invasiva.
Tras el alta hospitalaria se deberá realizar un seguimiento en un plazo de 2-4 semanas, en el que se deberá revisar el estado clínico del paciente, la resolución de la infección respiratoria, la cumplimentación, la técnica inhalatoria y la necesidad de OCD.
En todos los pacientes que no dispongan de espirometría previa, se etiquetará el caso como “Posible EPOC”. Se deberá realizar una espirometría de confirmación en fase de estabilidad.